题目内容
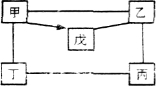
【题目】(8分)甲、乙、丙、丁、戊分别是稀硫酸、镁、氢氧化钠溶液、氧化镁及硫酸铜溶液中的一种。下图反映了它们之间的相互关系。其中“一”表示相连的物质间可以相互反应,“→”表示甲在一定条件下可以转化为戊。已知丁溶液呈蓝色。请回答以下问题:
(1)写出下列物质(或溶质)的化学式:
甲 、戊 。
(2)图中各反应不含有四种基本反应类型中的 反应。
(3)写出下列反应的化学方程式:
乙与丙: 。
丙与丁: 。
(4)例举丙在生产、生活中的一种用途: 。
【答案】(1)Mg;MgO (2)分解反应,
(3)2NaOH +H2SO4== Na2SO4+2H2O;CuSO4 +2NaOH== Cu(OH)2↓ + Na2SO4;
(4)氢氧化钠广泛应用于肥皂,石油、造纸、纺织和印染等工业。
【解析】
试题分析:(1)丁溶液呈蓝色,则丁为硫酸铜溶液,甲在一定条件下能转化为戊,则甲镁,戊为氧化镁,甲能和乙反应,则乙为硫酸,丙为氢氧化钠。(2)硫酸铜和镁反应生成铜和硫酸镁,属于置换反应;硫酸铜和氢氧化钠反应,生成氢氧化铜和硫酸钠,属于复分解反应,镁和氧气生成氧化镁,属于化合反应,故不含的基本反应类型为分解反应。
(3)乙与丙反应的化学方程式为:2NaOH +H2SO4== Na2SO4+2H2O;丙与丁反应的化学方程式为:CuSO4 +2NaOH== Cu(OH)2↓ + Na2SO4;(4)氢氧化钠广泛应用于肥皂,石油、造纸、纺织和印染等工业。

练习册系列答案
相关题目