题目内容
【题目】根据下列装置图填写有关空格: 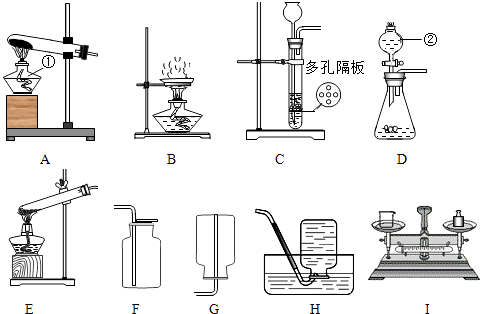
(1)装置A中仪器①的名称为;装置D中仪器②的名称为 .
(2)用稀硫酸和锌粒制氢气的发生装置可选用上述或(填序号)装置;收集氢气可用或(填序号)装置.
(3)除去粗盐中不溶性杂质的实验步骤是、过滤和蒸发结晶,用到的蒸发装置是 . (填序号),还必须用下列玻璃仪器组合中的(填序号)才能完成实验. ①漏斗、烧杯、玻璃棒 ②滴管、量筒、试管 ③集气瓶、表面皿、广口瓶
(4)用氯化钠固体和水配制5%的氯化钠溶液,需要用到上图装置中的(填序号). 若配制过程中,在已经有少量水的烧杯中加入5g氯化钠和95mL水,其他操作均规范,则所得溶液中氯化钠的质量分数(填“>”或“<”,或“=”)5%.
【答案】
(1)酒精灯;分液漏斗
(2)C;D;G;H
(3)溶解;B;①
(4)I;<
【解析】解:(1)图中装置A中仪器①的名称为酒精灯,装置D中仪器②的名称为分液漏斗.所以答案是:酒精灯、分液漏斗;(2)用稀硫酸和锌粒制氢气是固液不加热反应,图中CD适合固液不加热反应;氢气的密度小于空气的密度,并且不易溶于水,我们可以用排水法和向下排空气法收集.所以答案是:C或D、G或H;(3)要除去粗盐中不溶性杂质可以用过滤的方法,滤前要先溶解;蒸发时可用酒精灯加热,蒸发皿作反应容器,还有铁架台,所以可以用装置B做反应容器;过滤、溶解、蒸发所用的玻璃仪器有:烧杯、漏斗、玻璃棒,故可选①.所以答案是:溶解、B、①;(4)用氯化钠固体和水配制5%的氯化钠溶液,要经过计算、称量、溶解几个步骤,要用到图中的I;根据公式:溶液的溶质质量分数= ![]() ×100%可知,在已经有少量水的烧杯中加入5g氯化钠和95mL水,则所得溶液中氯化钠的质量分数小于5%.所以答案是:I、<.
×100%可知,在已经有少量水的烧杯中加入5g氯化钠和95mL水,则所得溶液中氯化钠的质量分数小于5%.所以答案是:I、<.
【考点精析】认真审题,首先需要了解蒸发操作的注意事项(蒸发注意点:1、在加热过程中,用玻璃棒不断搅拌2、当液体接近蒸干(或出现较多量固体)时停止加热,利用余热将剩余水分蒸发掉,以避免固体因受热而迸溅出来.3、热的蒸发皿要用坩埚钳夹取,热的蒸发皿如需立即放在实验台上,要垫上石棉网),还要掌握氢气的制取和检验(氢气的实验室制法原理:Zn + H2SO4 = ZnSO4 +H2↑;Zn + 2HCl = ZnCl2 +H2↑不可用浓盐酸的原因 浓盐酸有强挥发性 ;不可用浓硫酸或硝酸的原因 浓硫酸和硝酸有强氧化性)的相关知识才是答题的关键.