题目内容
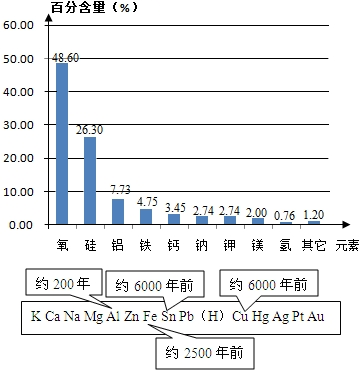
金属是一种重要的材料,人类的生活和生产都离不开金属,高科技新材料的开发和应用也需要金属.下图表示了金属活动性顺序表中铜、锡、铁和铝元素被人类大规模开发、利用的大致年限.

(1)你认为金属大规模开发、利用的先后顺序跟下列哪些因素有关(填序号)______
①地壳中金属元素的含量 ②金属的导电性 ③金属的活动性
④金属的延展性 ⑤金属冶炼的难易程度
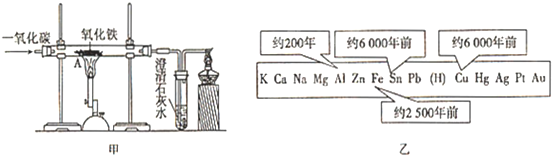
(2)能证明一氧化碳与氧化铁的反应产物中含有铁粉的简易方法是:______.
(3)“纳米α-Fe粉”,可以用于食品保鲜,称之为“双吸剂”,它能够吸收空气中的______和______.
(4)铝的活动性比铁强,但铝在空气中却表现出良好的抗蚀性,其原因是什么?(用化学方程式表示)______
(5)日常使用的金属材料多数属于合金.下表列出了一些常见合金的主要成分和性能.由表可推断,与组成合金的纯金属相比,合金的优点一般有(填编号)______:
①强度更好 ②硬度更大 ③熔点更低 ④抗腐蚀性能更优良
| 合金 | 合金的主要性能 | 主要成分及纯金属的性能 |
| 焊锡 | 熔点183℃ | 锡:熔点232℃;铅:熔点327℃. |
| 硬铝 | 强度和硬度好 | 铝、铜、镁等.硬度小,质软. |
| 不锈钢 | 抗腐蚀性好 | 铁、铬、镍等.纯铁易生锈. |
解:(1)金属被大规模开发、利用主要和金属的活动性有关,活动性弱的金属容易以单质形式存在,易被开发和利用,活泼金属一般以化合物形式存在,有的还比较难冶炼,其次是与该金属在地壳中的含量有关,含量越大,越容易被发现利用.分析所给的选项可以知道①③⑤是正确的;
(2)将反应后的物质加入适量稀盐酸中,若产生气泡则证明产生了铁粉;
(3)铁在空气中锈蚀的原理是铁与水和空气同时反应的结果,所以“纳米α-Fe粉”,可以用于食品保鲜,称之为“双吸剂”,它能够吸收空气中的氧气和水;
(4)铝的活动性比铁强,但铝在空气中却表现出良好的抗腐蚀性,是因为铝容易与空气中的氧气发生反应,会生成一层致密的氧化铝膜覆盖在铝的表面,阻止反应的进行,所以具有良好的抗腐蚀性所发生的反应为:2Al+3O2═Al2O3;
(5)比较表中的数据可分析出金属和合金的优缺点可以知道,合金一般比其成分金属的强度增大,硬度变大,熔点降低,抗腐蚀性能增强,故选①②③④.
故答案为:(1)①③⑤;
(2)将反应后的物质加入适量稀盐酸中,若产生气泡则证明产生了铁粉;
(3)氧气;水;
(4)2Al+3O2═Al2O3;
(5)①②③④.
分析:(1)从人类大规模开发、利用金属的年限可以看出,越活泼的金属,开发利用的越晚,说明主要和金属的活动性有关,另外,还与金属在地壳中的含量及冶炼的难以程度有关;
(2)铁可以和盐酸反应生成气体,可以据此进行判断;
(3)铁在空气中锈蚀的原理是铁与水和空气同时反应的结果;
(4)铝的活动性比铁强,但比铁耐腐蚀,要从形成保护膜角度考虑;
(5)比较表中的数据可分析出金属和合金的优缺点,解答时注意结合题给的选项来进行分析.
点评:解答这类题目时,首先,要熟记和理解金属活动性顺序及其应用,以及与之相关的知识等;然后,根据所给的实验、问题情景或图表信息等,结合所学的相关知识和技能,以及从生活、电视、网络中了解到的有关金属及合金的信息,细致地阅读、分析题意等,联系着生活实际,细心地进行探究、推理,最后,按照题目的要求,认真地进行选择或解答即可.
(2)将反应后的物质加入适量稀盐酸中,若产生气泡则证明产生了铁粉;
(3)铁在空气中锈蚀的原理是铁与水和空气同时反应的结果,所以“纳米α-Fe粉”,可以用于食品保鲜,称之为“双吸剂”,它能够吸收空气中的氧气和水;
(4)铝的活动性比铁强,但铝在空气中却表现出良好的抗腐蚀性,是因为铝容易与空气中的氧气发生反应,会生成一层致密的氧化铝膜覆盖在铝的表面,阻止反应的进行,所以具有良好的抗腐蚀性所发生的反应为:2Al+3O2═Al2O3;
(5)比较表中的数据可分析出金属和合金的优缺点可以知道,合金一般比其成分金属的强度增大,硬度变大,熔点降低,抗腐蚀性能增强,故选①②③④.
故答案为:(1)①③⑤;
(2)将反应后的物质加入适量稀盐酸中,若产生气泡则证明产生了铁粉;
(3)氧气;水;
(4)2Al+3O2═Al2O3;
(5)①②③④.
分析:(1)从人类大规模开发、利用金属的年限可以看出,越活泼的金属,开发利用的越晚,说明主要和金属的活动性有关,另外,还与金属在地壳中的含量及冶炼的难以程度有关;
(2)铁可以和盐酸反应生成气体,可以据此进行判断;
(3)铁在空气中锈蚀的原理是铁与水和空气同时反应的结果;
(4)铝的活动性比铁强,但比铁耐腐蚀,要从形成保护膜角度考虑;
(5)比较表中的数据可分析出金属和合金的优缺点,解答时注意结合题给的选项来进行分析.
点评:解答这类题目时,首先,要熟记和理解金属活动性顺序及其应用,以及与之相关的知识等;然后,根据所给的实验、问题情景或图表信息等,结合所学的相关知识和技能,以及从生活、电视、网络中了解到的有关金属及合金的信息,细致地阅读、分析题意等,联系着生活实际,细心地进行探究、推理,最后,按照题目的要求,认真地进行选择或解答即可.

练习册系列答案
 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案
相关题目