题目内容
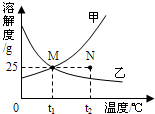 右下图为甲、乙两种固体物质在水中的溶解度曲线.
右下图为甲、乙两种固体物质在水中的溶解度曲线.
(1)______℃时,甲、乙两物质的溶解度相等.
(2)将水、甲的饱和溶液、乙的饱和溶液三种物质同时放入冰箱一段时间后,水和另一种物质里有晶体析出,这种物质是______.
(3)t1℃时,将30g 乙物质加入到100g水中充分溶解,所形成溶液是______溶液(填“饱和”或“不饱和”);其溶质质量分数是______.
解:由甲、乙两种固体物质在水中的溶解度曲线图可知:
(1)t1℃时,甲、乙两物质的溶解度相等.
(2)将水、甲的饱和溶液、乙的饱和溶液三种物质同时放入冰箱一段时间后,水和另一种物质里有晶体析出,这种物质是溶解度随着温度的升高溶解度增加的物质甲.
(3)由图可知:t1℃时,二者溶解度都为25克,将30g 乙物质加入到100g水中充分溶解,所形成溶液是饱和溶液;其溶质质量分数是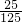 ×100%=20%.
×100%=20%.
故答为:(1)t1℃. (2)甲.(3)饱和; 20%.
分析:由甲、乙两种固体物质在水中的溶解度曲线图可知:
(1)掌握溶解度曲线图中交点的意义,则可知:t1℃时,甲、乙两物质的溶解度相等.
(2)将水、甲的饱和溶液、乙的饱和溶液三种物质同时放入冰箱一段时间后,水和另一种物质里有晶体析出,则为溶解度随着温度的升高溶解度增加的物质.
(3)由图可知:t1℃时,二者溶解度都为25克,将30g乙物质加入到100g水中充分溶解,所形成溶液是否饱和;可求其溶质质量分数.
点评:溶解度曲线能定量地表示出溶解度变化的规律,从溶解度曲线可以看出:同一溶质在不同温度下的溶解度;同一温度下,不同溶质的溶解度;温度对不同物质的溶解度影响不同.
(1)t1℃时,甲、乙两物质的溶解度相等.
(2)将水、甲的饱和溶液、乙的饱和溶液三种物质同时放入冰箱一段时间后,水和另一种物质里有晶体析出,这种物质是溶解度随着温度的升高溶解度增加的物质甲.
(3)由图可知:t1℃时,二者溶解度都为25克,将30g 乙物质加入到100g水中充分溶解,所形成溶液是饱和溶液;其溶质质量分数是
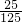 ×100%=20%.
×100%=20%.故答为:(1)t1℃. (2)甲.(3)饱和; 20%.
分析:由甲、乙两种固体物质在水中的溶解度曲线图可知:
(1)掌握溶解度曲线图中交点的意义,则可知:t1℃时,甲、乙两物质的溶解度相等.
(2)将水、甲的饱和溶液、乙的饱和溶液三种物质同时放入冰箱一段时间后,水和另一种物质里有晶体析出,则为溶解度随着温度的升高溶解度增加的物质.
(3)由图可知:t1℃时,二者溶解度都为25克,将30g乙物质加入到100g水中充分溶解,所形成溶液是否饱和;可求其溶质质量分数.
点评:溶解度曲线能定量地表示出溶解度变化的规律,从溶解度曲线可以看出:同一溶质在不同温度下的溶解度;同一温度下,不同溶质的溶解度;温度对不同物质的溶解度影响不同.

练习册系列答案
 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案
相关题目
已知某氯化钠样品中含有少量的碳酸钠固体.氯化钠与稀盐酸不发生化学反应,碳酸钠与稀盐酸反应生成氯化钠、水和二氧化碳.甲、乙、丙三同学分别对其成分进行测定,有关实验数据如下表(烧杯的质量为35.00g).
| 甲 | 乙 | 丙 | |
| (烧杯+稀盐酸)的质量 | 75.00g | 85.00g | 75.00g |
| 加入氯化钠样品的质量 | 4.00g | 4.00g | 6.00g |
| 充分反应后(烧杯+剩余物)的质量 | 78.56g | 88.56g | 80.56g |
(2)求样品中氯化钠的质量分数.
(3)求恰好完全反应后所得溶液的溶质的质量分数.
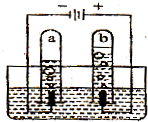 如图所示是电解水的简易装置,请回答下列问题
如图所示是电解水的简易装置,请回答下列问题 ______+______,该反应属于______.(填“化合反应”或“分解反应”)
______+______,该反应属于______.(填“化合反应”或“分解反应”)