题目内容
【题目】请结合下列实验装置图回答有关问题。
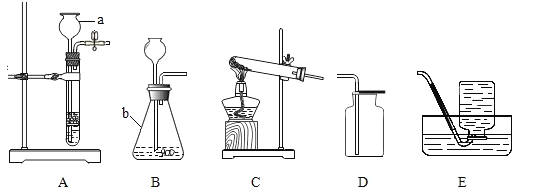
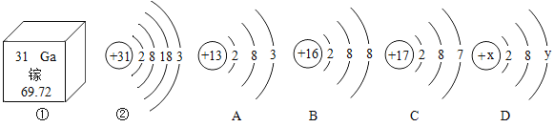
①仪器a的名称________,b的名称________.
②用加热高锰酸钾固体制取并收集一瓶较纯净的氧气,可选择的装置组合:___(填字母),如果用装置B制取氧气,则发生反应的化学方程式为________
③实验室制取二氧化碳气体,装置A. B都可用作发生装置,其中可以控制反应进行的是________。(填装置序号),反应的化学方程式是________。
④待石灰石和一定量的稀盐酸反应至气泡逸出不明显后,某兴趣小组同学测得其残留液pH等于2,由此得出残留液中除含有氯化钙外,还含有盐酸。为验证是否含有盐酸,他们采用不同方案进行实验,得出相同的结论。
实验操作 | 实验现象 | 结论 | |
方案一 | 取样,滴加过量的碳酸钠溶液 | ________ | 有盐酸 |
方案二 | 取样,滴加AgNO3溶液和稀硝酸的混合溶液 | 产生白色沉淀 |
上述实验方案中,合理的是___(选填:“方案一”或“方案二”);另外一个实验方案不合理的原因:________。“方案一”中反应的化学方程式为________。
【答案】长颈漏斗 锥形瓶 CE 2H2O2![]() 2H2O+O2↑ A CaCO3+2HCl=CaCl2+H2O+CO2↑ 先有气泡冒出,再有白色沉淀生成 方案一 氯化钙和硝酸银反应也生成氯化银白色沉淀 Na2CO3+2HCl═2NaCl+H2O+CO2↑,CaCl2+Na2CO3═CaCO3↓+2NaCl
2H2O+O2↑ A CaCO3+2HCl=CaCl2+H2O+CO2↑ 先有气泡冒出,再有白色沉淀生成 方案一 氯化钙和硝酸银反应也生成氯化银白色沉淀 Na2CO3+2HCl═2NaCl+H2O+CO2↑,CaCl2+Na2CO3═CaCO3↓+2NaCl
【解析】
(1)长颈漏斗方便加液体药品,锥形瓶是常用的反应容器;故答案为:长颈漏斗;锥形瓶;
(2)用高锰酸钾制氧气,反应物是固体,需要加热;氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集,排水法收集收集的氧气比较纯净,用加热高锰酸钾固体制取并收集一瓶较纯净的氧气,可选择的装置组合CE;如果用装置B制取氧气,所用药品为过氧化氢溶液和二氧化锰,过氧化氢在二氧化锰催化作用下分解生成水和氧气,发生反应的化学方程式为:2H2O2![]() 2H2O+O2↑;
2H2O+O2↑;
(3)实验室制取二氧化碳气体,装置A. B都可用作发生装置,其中可以控制反应进行的是A,因为通过控制止水夹,可能实现固体与液体的分离;如果用装置B制取氧气,B中没有酒精灯,是过氧化氢在二氧化锰催化作用下生成水和氧气,实验室制取二氧化碳气体,是用大理石或石灰石与稀盐酸,大理石和石灰石的主要成分是碳酸钙,碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑;
(4)方案一,取样,滴加碳酸钠溶液至过量,先有气泡冒出,再有白色沉淀生成,说明有盐酸,盐酸和碳酸钠反应生成氯化钠、二氧化碳和水,氯化钙和碳酸钠反应生成碳酸钙沉淀和氯化钠;上述实验方案中,合理的是方案一;另外一个实验方案不合理的原因:氯化钙和硝酸银反应也生成氯化银白色沉淀;故答案为:先有气泡冒出,再有白色沉淀生成;方案一;氯化钙和硝酸银反应也生成氯化银白色沉淀;Na2CO3+2HCl═2NaCl+H2O+CO2↑,CaCl2+Na2CO3═CaCO3↓+2NaCl。

 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案【题目】小红同学进行酸碱中和反应的实验(如图所示)。她向氢氧化钠溶液中滴加一定量稀盐酸后,想起氢氧化钠溶液中事先没有滴加指示剂。为了确定盐酸与氢氧化钠的反应程度,她从烧杯中取了少量溶液于试管中,并向试管中滴加几滴无色酚酞试液,振荡,观察到试管中液体颜色没有变化。于是她对烧杯中的溶液进行了以下探究:

(1)小红认为此时烧杯中的溶液可能有以下三种情况:
①盐酸与氢氧化钠恰好完全反应;②氢氧化钠有剩余;③盐酸有剩余
小明同学却判定不可能“氢氧化钠有剩余”,他的理由是 。
(2)他们共同设计了一个实验方案,欲对上述其他两种可能情况进行验证。请根据相关内容填写下表:
实验方法 | 可能观察到的现象 | 结论 |
将少量锌粒放入试管中,然后从烧杯中取适量溶液至试管中 | 如果 | 则盐酸过量 |
如果 | 则盐酸与氢氧化钠恰好完全反应 |
(3)经过讨论,他们认为利用下列几种物质代替锌粒,也可以达到验证目的,你认为其中不正确的是 (填序号)。
A.生锈的铁钉 B.碳酸钠粉末 C.硫酸钠粉末 D.氢氧化铜
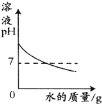
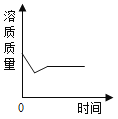
(4)下列曲线能够表示小红所做实验中溶液pH变化趋势的是 (填序号)。