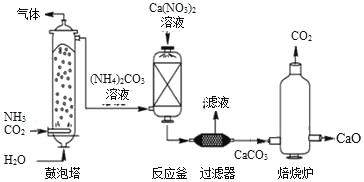
题目内容
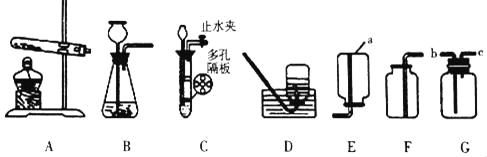
【题目】根据图1实验装置图,回答有关问题。
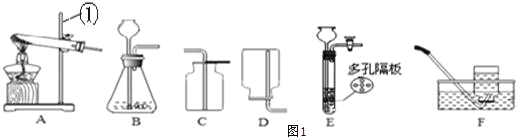
(1)写出标号①的仪器名称:__________;
(2)实验室用氯酸钾制取O2的化学方程式为__________;收集O2选择的装置是__________(填字母)。氯酸钾制取氧气完全反应后的固体残渣,通过以下操作可回收得到较纯的二氧化锰(残渣中只有二氧化锰难溶于水)。正确操作的先后顺序是__________(填写选项符号)。
a.烘干b。溶解c。过滤d。洗涤
(3)用大理石和稀盐酸制取二氧化碳,可选用的装置组合为__________,E装置相对于B装置有的优点是___________;并写出该反应的化学方程式__________。
(4)为了验证二氧化碳与氢氧化钠可以发生化学反应,某兴趣小组用图2所示装置进行实验,请分析回答下列问题:
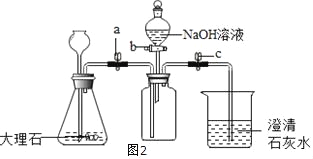
①打开止水夹a和c,关闭b,从长颈漏斗中加入足量的稀盐酸,当观察到__________,说明集气瓶中已集满二氧化碳气体,然后待锥形瓶中反应停止后,关闭a,打开b,滴入足量氢氧化钠溶液后关闭活塞b,一段时间后可观察到__________,证明二氧化碳与氢氧化钠发生了化学反应。
②小红认为仅做上述实验有不足之处,可再利用如图装置做一个对比实验即可证明,该对比实验只需将所用的氢氧化钠溶液换成__________即可。
③小明认为要想证明二氧化碳与氢氧化钠溶液确实发生了反应,也可取反应后的溶液少许,滴加__________,根据现象即可判断。
【答案】铁架台;2KClO3![]() 2KCl+3O2↑;C或F;bcda;BC或EC;可以控制反应的发生和停止;CaCO3+2HCl=CaCl2+H2O+CO2↑;澄清石灰水浑浊;烧杯中浑浊液体倒吸入集气瓶中;水;稀盐酸(或氯化钙溶液或是氢氧化钙溶液等)。
2KCl+3O2↑;C或F;bcda;BC或EC;可以控制反应的发生和停止;CaCO3+2HCl=CaCl2+H2O+CO2↑;澄清石灰水浑浊;烧杯中浑浊液体倒吸入集气瓶中;水;稀盐酸(或氯化钙溶液或是氢氧化钙溶液等)。
【解析】
(1)标号①的仪器名称是铁架台。
(2)氯酸钾在二氧化锰做催化剂和加热的条件下生成氯化钾和氧气,反应方程式为2KClO3![]() 2KCl+3O2↑;氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法C和排水法F收集;回收得到较纯净的二氧化锰操作步骤是:溶解、过滤、洗涤、烘干,故顺序为bcda。
2KCl+3O2↑;氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法C和排水法F收集;回收得到较纯净的二氧化锰操作步骤是:溶解、过滤、洗涤、烘干,故顺序为bcda。
(3)实验室制取二氧化碳属于固液常温型,所以制取装置可选择B或E,二氧化碳的密度比空气大,能溶于水,所以可用向上排空气法装置C来收集,故组合装置为BC或EC;在实验室用大理石和稀盐酸制取CO2的实验装置中,F装置相对于B装置具有的优点是:可以控制反应的发生和停止;碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,反应方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑;
(4)①打开止水夹a和c,关闭b,从长颈漏斗中加入足量的稀盐酸,大理石与稀盐酸反应生成二氧化碳,二氧化碳气体的密度比空气大,且能够使澄清的石灰水变浑浊,若观察到烧杯中澄清的石灰水变浑浊,说明二氧化碳已经收集满;关闭a,打开b,滴入足量氢氧化钠溶液后关闭活塞b,二氧化碳与氢氧化钠反应造成集气瓶内的压强减小,一段时间后可观察到烧杯中的浑浊液体倒吸入集气瓶内,证明二氧化碳与氢氧化钠发生了化学反应。
②二氧化碳和氢氧化钠反应生成碳酸钠和水,但是二氧化碳和水反应非常微小(可以不于考虑)。这样一比较可以发现,倒吸是由二氧化碳和氢氧化钠反应造成的;③根据二氧化碳和氢氧化钠溶液反应后的产物可以知道,若反应则生成了碳酸钠,所以可以检验是否存在碳酸钠来判断反应是否发生,可以选择稀盐酸、氯化钙溶液或是氢氧化钙溶液等来进行验证;

【题目】某同学在实验室用氯酸钾和二氧化锰混合物制取氧气,充分反应后,并对反应后的固体物质进行回收利用,实验数据如表,请回答下列问题:
实验前 | 实验后 |
试管内固体物质的质量 | 试管内固体物质的质量 |
18.0g | 13.2g |
(1)得到氧气多少克________?
(2)最多能回收二氧化锰多少克________?
(3)回收后的一种物质可以作肥料,它属于______肥,要回收反应后的物质需要用到操作有哪些?
【题目】完成如表并回答下列问题
试管编号 | 加入液体 | 加入物质 | 实验现象 |
|
| 一滴植物油 | _____________ |
|
| 一滴植物油 | _____________ |
|
| 几小粒碘 | _____________ |
|
| 几小粒碘 | _____________ |
注意:“实验现象”填“溶解”或“不溶解”即可.
![]() 上述实验说明同一物质在________的溶剂中溶解的能力________.
上述实验说明同一物质在________的溶剂中溶解的能力________.
![]() 为什么汽油可用来清除衣服上的油渍______?
为什么汽油可用来清除衣服上的油渍______?
![]() 除去衣服上的油渍,用汽油洗和用洗涤剂洗其原理是否相同_______?
除去衣服上的油渍,用汽油洗和用洗涤剂洗其原理是否相同_______?