题目内容
【题目】下表是甲、乙、丙三种物质的部分溶解度(单位:g/100g水),请回答。
温度(℃) | 10 | 20 | 30 | 40 | 50 | 60 |
甲 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
乙 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110.0 |
丙 | 0.182 | 0.165 | 0.160 | 0.141 | x | 0.121 |
① 10℃时,甲物质的溶解度是g/100g水;
② 三种物质中溶解度受温度影响较大的是;
③ 物质在水中的溶解性与其溶解度(20℃)的关系示意图如下,则丙物质在水中的溶解性是;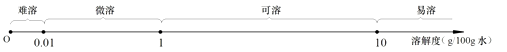
④ 30℃时,乙物质饱和溶液的溶质质量分数是;(列式即可,不要求计算)
⑤ 50℃时,三种物质的溶解度由大到小的顺序是;
⑥ 向不同温度的100 g水中分别放入等质量的乙物质,保持温度不变,溶解情况如图所示。相关分析正确的是;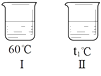
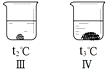
a.溶液温度:Ⅰ>Ⅱ>Ⅲ>Ⅳ
b.溶液质量:Ⅰ=Ⅱ>Ⅲ>Ⅳ
c.溶液Ⅰ一定是不饱和溶液
d.使Ⅳ中的固体全部溶解,溶质质量分数可能不变
【答案】35.8;乙;微溶于水;![]() ;乙、甲、丙;bd
;乙、甲、丙;bd
【解析】①从表中数据可知10℃时,甲的溶解度是35.8g;
②从表中数据可知乙物质的溶解度受温度影响较大;
③丙物质在20℃时,溶解度为0.165g,在0.01~1g之间,属于微溶于水;
④30℃时,乙物质饱和溶液的溶质质量分数是45.8÷(45.8g+100g)×100%;
⑤从表中数据可知50℃时,甲、乙、丙三种物质的溶解度分别为:37g、85g、0.141g与0.121之间,故50℃时,三种物质的溶解度由大到小依次为乙、甲、丙;
⑥乙物质溶解度随温度升高而增大,
a、由于Ⅰ、Ⅱ的溶液均无固体,无法判断其温度情况,故错误;b、100g水中分别放入等质量的乙物质,由于Ⅰ、Ⅱ中均无固体,溶液的质量相同,Ⅲ中固体小于Ⅳ,所以溶液的质量Ⅲ>Ⅳ,所以溶液质量:Ⅰ=Ⅱ>Ⅲ>Ⅳ,故正确;c、由于不知道加入乙物质的质量,无法判断溶液是否饱和,故错误;d、使Ⅳ中的固体全部溶解,如果温度不变,加入适量水,恰好达到饱和时,溶质质量分数不变,选bd.
所以答案是::①35.8;②乙;(3)微溶于水;(4)![]() ×100%;(5)乙、甲、丙;(6)bd.
×100%;(5)乙、甲、丙;(6)bd.
【考点精析】解答此题的关键在于理解饱和溶液和不饱和溶液的相关知识,掌握饱和与不饱和的判断方法:看有无不溶物或继续加入该溶质,看能否溶解,以及对固体溶解度的影响因素的理解,了解影响固体溶解度的因素:①溶质、溶剂的性质(种类) ②温度:大多数固体物的溶解度随温度升高而升高;如KNO3;少数固体物质的溶解度受温度的影响很小;如NaCl;极少数物质溶解度随温度升高而降低.如Ca(OH)2.

 阅读快车系列答案
阅读快车系列答案