题目内容
 铁是生产、生活中应用最广泛的一种金属.以下是初中化学有关铁的性质的一些基本实验:
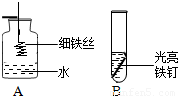
铁是生产、生活中应用最广泛的一种金属.以下是初中化学有关铁的性质的一些基本实验:(1)某同学用向上排空气法收集一瓶氧气做A实验,在引燃的火柴快燃尽时将细铁丝插入集气瓶中,未观察到剧烈燃烧,火星四射现象,其原因可能是______(写出一条).
若B中为稀盐酸,观察到的现象是______.
若B中为硫酸铜溶液,反应的化学方程式为______.
(2)通过以上实验你得出的结论是______.
【答案】分析:(1)根据铁丝在氧气中燃烧的实验方面进行分析、判断,从而得出正确的结论;
根据铁与稀盐酸反应的现象,进行分析解答;
根据书写化学方程式的步骤:写配注等,写出反应方程式即可;
(2)根据金属的性质、金属活动性顺序知识进行总结.
解答:解:(1)“铁丝在氧气中燃烧”的实验,有时看不到预期的实验现象,有以下几个原因:
①集气瓶内氧气的浓度太低,不足以使铁丝燃烧或剧烈燃烧、火星四射.
【导致氧气的浓度低的原因:I、可能是利用排气法而收集到氧气的纯度低;Ⅱ、可能未等火柴燃烧尽就插入盛氧气的集气瓶中,火柴继续燃烧消耗了一定量的氧气,同时有大量的热量放出,使瓶内氧气膨胀逸出;Ⅲ、也可能将系着快燃尽的火柴的铁丝迅速伸至集气瓶底部,燃烧产生的热量使氧气膨胀逸出.】
②铁丝太粗,与氧气的接触面积太小,使铁丝不能燃烧或不能充分燃烧.
③铁丝表面生锈了而未打磨除去.
铁与稀盐酸反应的现象为:铁钉表面产生气泡,溶液由无色变为浅绿色;
铁钉与硫酸铜溶液反应的化学方程式为:Fe+CuSO4=FeSO4+Cu;
(2)通过以上实验你得出的结论是:铁是一种化学性质比较活泼的金属;
故答案为:(1)铁丝表面有铁锈(或集气瓶中氧气含量少);
铁钉表面产生气泡,溶液由无色变为浅绿色;
Fe+CuSO4=FeSO4+Cu;
(2)铁是一种化学性质比较活泼的金属.
点评:并非每个实验都能成功,会做实验的同时,还要学会分析实验失败的原因.熟记和理解金属的性质及用途、常见金属的特性及其应用、金属活动性顺序及其应用等相关知识,才能顺利解题.
根据铁与稀盐酸反应的现象,进行分析解答;
根据书写化学方程式的步骤:写配注等,写出反应方程式即可;
(2)根据金属的性质、金属活动性顺序知识进行总结.
解答:解:(1)“铁丝在氧气中燃烧”的实验,有时看不到预期的实验现象,有以下几个原因:
①集气瓶内氧气的浓度太低,不足以使铁丝燃烧或剧烈燃烧、火星四射.
【导致氧气的浓度低的原因:I、可能是利用排气法而收集到氧气的纯度低;Ⅱ、可能未等火柴燃烧尽就插入盛氧气的集气瓶中,火柴继续燃烧消耗了一定量的氧气,同时有大量的热量放出,使瓶内氧气膨胀逸出;Ⅲ、也可能将系着快燃尽的火柴的铁丝迅速伸至集气瓶底部,燃烧产生的热量使氧气膨胀逸出.】
②铁丝太粗,与氧气的接触面积太小,使铁丝不能燃烧或不能充分燃烧.
③铁丝表面生锈了而未打磨除去.
铁与稀盐酸反应的现象为:铁钉表面产生气泡,溶液由无色变为浅绿色;
铁钉与硫酸铜溶液反应的化学方程式为:Fe+CuSO4=FeSO4+Cu;
(2)通过以上实验你得出的结论是:铁是一种化学性质比较活泼的金属;
故答案为:(1)铁丝表面有铁锈(或集气瓶中氧气含量少);
铁钉表面产生气泡,溶液由无色变为浅绿色;
Fe+CuSO4=FeSO4+Cu;
(2)铁是一种化学性质比较活泼的金属.
点评:并非每个实验都能成功,会做实验的同时,还要学会分析实验失败的原因.熟记和理解金属的性质及用途、常见金属的特性及其应用、金属活动性顺序及其应用等相关知识,才能顺利解题.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案
相关题目
 16、铁是生产、生活中应用最广泛的一种金属.以下是初中化学有关铁的性质的一些基本实验:
16、铁是生产、生活中应用最广泛的一种金属.以下是初中化学有关铁的性质的一些基本实验: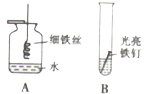
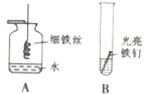
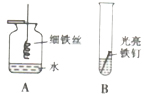
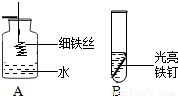 铁是生产、生活中应用最广泛的一种金属.以下是初中化学有关铁的性质的一些基本实验:
铁是生产、生活中应用最广泛的一种金属.以下是初中化学有关铁的性质的一些基本实验: