题目内容
【题目】实验是进行科学探究的重要手段。请回答下列问题。

(1)实验A排水法收集气体,集气瓶内装满水的目的是___。
(2)实验B集气瓶中预先加水的目的 ___,待火柴即将燃尽时,将铁丝由上而下___(填“缓慢”或“迅速”)伸入盛有集满氧气的集气瓶中。
(3)实验C 出现的现象是______,原因是______(用化学方程式)。
(4)实验D现象是________,由此说明二氧化碳的性质_________。
【答案】收集气体更纯 防止反应生成的高温熔化物溅落瓶底,使集气瓶炸裂 缓慢 纸花变成红色 H2O + CO2= H2CO3 蜡烛从下往上依次熄灭 不能燃烧不支持燃烧,密度大于空气
【解析】
(1)集气瓶内装满水可以排净瓶内的空气,使收集的气体更纯净,故填收集气体更纯;
(2)集气瓶中预先加水的可以防止反应中生成的高温熔化物溅落瓶底,使集气瓶炸裂,故填防止反应中生成的高温熔化物溅落瓶底,使集气瓶炸裂;
做铁丝在氧气中燃烧时,应将铁丝由上而下缓慢伸入到盛有集满氧气的集气瓶中,使铁丝与氧气充分接触反应,现象明显,故填缓慢。
(3)赶到的现象是干燥的纸花由紫变红,故填纸花变成红色;
二氧化碳与水反应生成碳酸,故反应的化学方程式为:H2O + CO2= H2CO3。
(4)实验D现象是蜡烛从下往上依次熄灭,故填蜡烛从下往上依次熄灭;
蜡烛熄灭说明二氧化碳不能燃烧不支持燃烧;下层蜡烛先灭,上层蜡烛后灭,说明二氧化碳的密度大于空气的密度,故填不能燃烧不支持燃烧,密度大于空气。

 阅读快车系列答案
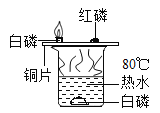
阅读快车系列答案【题目】某小组将光亮铜片放在酒精灯火焰上加热,发现表面变黑,他们对黑色物质来源展开探究。
(猜想假设)猜想1:黑色固体是酒精燃烧生成。
猜想2:黑色固体是铜与空气反应生成。
(查阅资料)
(1)酒精等含碳物质在氧气不充足时会燃烧生成炭黑,炭黑难溶于水,与稀硫酸不反应。
(2)氧化铜加热时能溶于稀硫酸生成蓝色溶液
(进行实验)
实验步骤和方法 | 实验现象 | 实验结论 |
实验一:取一小段光亮铜片,放入试管内,然后用试管夹夹持试管,放在酒精灯的外焰部位加热。 | 铜片表面_______(“变”或“不变”)黑。 | 猜想1不正确 |
实验二:另取一小段光亮铜片用金属铝严密包裹,压紧不留空隙,放在酒精灯的外焰部位加热一段时间后,打开包裹的铝箔,观察现象。 | 刚打开包裹的铝箔时铜片不变黑;一段时间后铜片变黑。 | 猜想2正确 |
实验三:再取一小段光亮铜片,在酒精灯火焰上加热变黑。然后把附着黑色固体的铜片投入到有稀硫酸的试管中,加热。 | 盛黑色固体全部溶解消失,溶液____。 | 猜想2正确 |
(反思拓展)
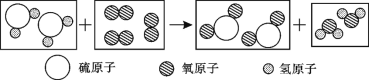
(1)请用符号表达式表示黑色物质的来源:_______;反应过程的微观示意图可简单表示如下,请在反应中方框内画出正确的图示。_______
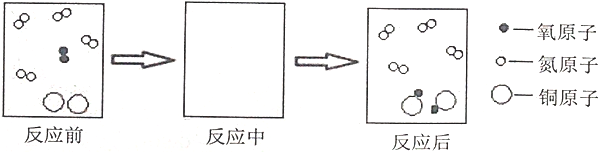
(2)实验二用金属铝箔将铜片严密包裏的目的是_______;
(3)实验方案的设计主要有从反应物和从生成物两个角度。上述实验主要从反应物角度设计的是______(填序号)
a.实验一 b.实验二 c.实验三