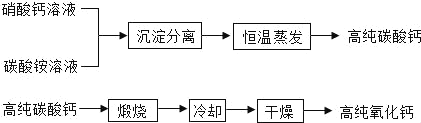
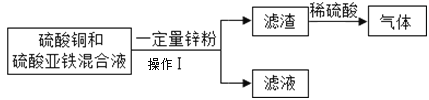
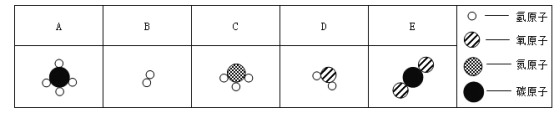
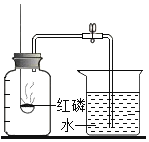
题目内容
【题目】某同学利用从废电池拆下的锌片制取氢气,他取20 g这种含杂质的锌片样品,放人100g稀硫酸中,二者恰好完全反应(杂质不与稀硫酸反应),反应后称得剩余混合物的总质量为119.6g. 请计算:
(1)反应生成氢气的质量是________________g。
(2)这种含杂质的锌片中锌的质量分数是___________?
(3)100g稀硫酸中H2SO4的质量是_________________g。
【答案】0.4 65% 19.6
【解析】
(1)由质量守恒定律可知:反应生成氢的质量=20g+100g+-119.6g=0.4g。
(2)设参加反应锌的质量为x,稀硫酸溶质质量为y
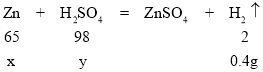
![]() ,
,![]()
解得:x=13g,y=19.6g
这种含杂质的锌片中锌的质量分数=![]() 。
。
(3)由(2)可知,100g稀硫酸中H2SO4的质量是19.6g。

练习册系列答案
 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案
相关题目
【题目】小强同学对样品中碳酸钙的质量分数进行检测,采用的办法如下:取用 8g 这种石灰石样品,把 40g 稀盐酸分 4 次加入,测量过程所得数据见下表(已知石 灰石样品中含的杂质不溶于水,不与盐酸反应).请计算:
序号 | 加入稀盐酸质量(g) | 剩余固体质量(g) |
第 1 次 | 10 | 5 |
第 2 次 | 10 | m |
第 3 次 | 10 | 1.2 |
第 4 次 | 10 | 1.2 |
(1)8g 石灰石样品中含有杂质多少克?
(2)样品中碳酸钙的质量分数是多少?
(3)下表中 m 的数值应该为多少?
(4)要得到 280kg CaO,需要质量分数为 80%的石灰石多少千克?(化学方程式:CaCO3  CaO+CO2↑)
CaO+CO2↑)