题目内容
【题目】(1)用氯化钠固体配制100 g溶质质量分数为12%的NaCl溶液的操作步骤为________、 ________ 、 ________ 、___________ 。如果将这100 g溶质质量分数为12%的NaCl溶液加水稀释为4%的NaCl溶液需加水_______ g。
(2)20 g黄铜(铜锌合金)与100 g稀硫酸恰好完全反应共产生0.4g氢气。
求:①合金中锌的质量分数_______。
②计算稀硫酸的质量分数_______。
【答案】计算 称量 溶解 装瓶存放 200 65% 19.6%
【解析】
(1)配制溶质为固体的一定溶质质量分数的溶液,操作步骤是计算、称量、溶解、装瓶存放,故填计算、称量、溶解、装瓶存放;
需要加入水的质量为![]() 100g=200g,故填200。
100g=200g,故填200。
(2)解:设合金中锌的质量为x,参加反应的纯硫酸的质量为y
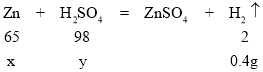
![]()
x=13g
![]()
y=19.6g
合金中锌的质量分数为![]() ×100%=65%
×100%=65%
稀硫酸中硫酸的质量分数为![]() ×100%=19.6%
×100%=19.6%
答:①合金中锌的质量分数为65%;
②稀硫酸的溶质质量分数为19.6%。

【题目】小明进行H2O2溶液制O2的实验探究。结合下列过程,回答有关问题。
(1)MnO2作催化剂,向5mL5%的H2O2溶液中加入少量MnO2,立即产生大量气泡。
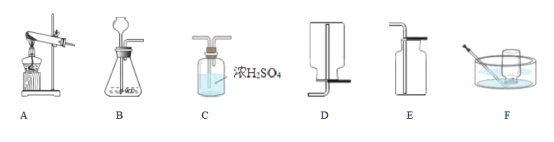
①写出用H2O2溶液制备O2的化学方程式:____________________________________。
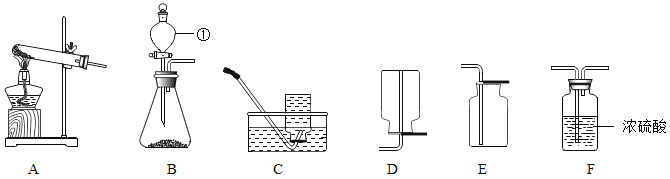
②用上述反应原理制备并收集一瓶干燥的O2,从所给装置图中选择并组装一套装置,其连接顺序为_______→ __________→ ________(填标号)。为了确保实验成功,在装药品之前应该_________。
③检验O2的方法是___________________________ ,若木条复燃,则证明收集的气体为O2。
(2)FeCl3溶液做催化剂
向5mL5%的H2O2溶液中加入2滴一定浓度的 FeCl3溶液,立即产生大量气泡。
(已知)FeCl3溶液中主要含有三种微粒:H2O、Fe3+、Cl-
(问题)那种微粒对H2O2溶液的分解起催化作用?
(假设)假设一:可能是H2O
假设二:可能是Fe3+
假设三:可能是Cl-
(分析)①假设一不可能成立,理由是__________________________________________。
(实验)
操作 | 现象 |
其他条件不变,向H2O2溶液中加入NaCl溶液 | 无明显变化 |
其他条件不变,向H2O2溶液中加入Na2SO4溶液 | 无明显变化 |
其他条件不变,向H2O2溶液中加入Fe2(SO4)3溶液 | 立即产生大量气泡 |
(结论)②假设___成立,而假设一和另一种假设不成立。
③催化剂比较从循环利用的角度分析,_____(填化学式)更适合做该反应的催化剂。