题目内容
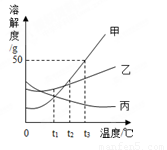
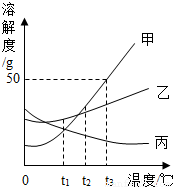
如图所示,依据甲、乙、丙三种固体物质的溶解度曲线,回答下列问题:

(1)t1℃时,甲、乙、丙三种物质的溶解度的关系是 (用>、<或=表示.
(2)t3℃时,甲物质饱和溶液中,溶质、溶剂、溶液的质量之比为 (填最简比).
(3)甲中含有少量的乙,若要提纯甲,可采用 的方法.
(4)t2℃时,甲、乙、丙三种物质的饱和溶液各100g,分别降温到t1℃时,所得溶液质量的关系是 (用>、<或=表示).
(1)乙>甲=丙(或甲=丙<乙);(2)1:2:3;(3)冷却热饱和溶液(或降温结晶);(4)丙>乙>甲(或甲<乙<丙).
【解析】
试题分析:(1)从t1℃向上做垂线,与曲线的交点在上面的溶解度就大,所以t1℃时它们的溶解度大小顺序是乙>甲=丙(或甲=丙<乙);
(2)t3℃时,甲物质的溶解度是50g,即100g水中最多溶解50g甲,所以t2℃时,甲物质饱和溶液中,溶质、溶剂、溶液的质量之比为:50g:100g:150g=1:2:3;
(3)如果溶解度受温度影响较大的物质从溶液中结晶析出的方法是冷却热饱和溶液,如果溶解度受温度影响不大的物质从溶液中结晶析出的方法是蒸发溶剂.由于甲的溶解度受温度影响较大,所以提纯甲用冷却热饱和溶液或降温结晶的方法;
(4)由于丙物质的溶解度随着温度的升高而减小,所以降温后溶解度变大,不会析出晶体,溶液质量不变,所以仍然是100g,从t2℃降到t1℃时,甲的溶解度减小的幅度大,所以甲析出的晶体比乙析出的晶体多,所以降温后甲溶液的质量最小,乙次之,丙溶液质量最大.
考点:固体溶解度曲线及其作用;结晶的原理、方法及其应用.
点评:解答本题关键是要知道溶解度大小的比较方法,能够根据溶解度定义解决一些问题,知道溶液中析出晶体的方法,熟悉物质提纯的方法.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 (2013?锦州)如图所示,依据甲、乙、丙三种固体物质的溶解度曲线,回答下列问题:
(2013?锦州)如图所示,依据甲、乙、丙三种固体物质的溶解度曲线,回答下列问题: