题目内容
化学用语是化学学科的专用语言,是我们学习化学的重要工具.(1)请从给定化合价的
| +1 |
| K |
| 0 |
| Cu |
| -2 |
| O |
| +5 |
| N |
| +1 |
| H |
金属单质
(2)下面是五种粒子的结构示意图:
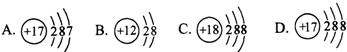
图中粒子共能表示
分析:(1)化合价为零的元素组成的物质为单质.金属单质的化学式用金属元素的元素符号表示;
化合价不是零的金属元素可以形成金属氧化物;
复合肥料是同时至少含有氮、磷、钾中两种元素的化合物.
(2)元素种类的判断依据是核内质子数;
核内质子数大于核外电子总数的是阳离子;
元素周期表中的行表示周期,第一周期有两种元素,第二周期有八种元素,第三周期也有八种元素.
化合价不是零的金属元素可以形成金属氧化物;
复合肥料是同时至少含有氮、磷、钾中两种元素的化合物.
(2)元素种类的判断依据是核内质子数;
核内质子数大于核外电子总数的是阳离子;
元素周期表中的行表示周期,第一周期有两种元素,第二周期有八种元素,第三周期也有八种元素.
解答:解:(1)所提供的元素中只有铜元素的化合价为零,能组成金属单质,即金属铜,其化学式用铜的元素符号Cu表示.
化合价不是零的金属元素只有+1价的钾元素,它形成的氧化物是氧化钾.其化学式的书写步骤如下:
第一步:写出元素符号,氧元素符号在右,碳元素符号在左:KO
第二步:标注元素的化合价:
第三步:化合价的绝对值交叉写在元素符号的右下角:K2O
第四步:用化合价原则检查:(+1)×2+(-2)=0
因此K2O就是钾的氧化物的化学式.
所提供的元素能形成的复合肥是硝酸钾.硝酸钾由+1价的钾元素和-1价的硝酸根构成,其化学式的书写步骤如下:
第一步:写出元素符号或原子团,正价元素或原子团的符号在左,负价元素或原子团的符号在右:KNO3
第二步:标注元素的化合价:
第三步:化合价的绝对值交叉写在元素符号的右下角:K1(NO3)1.数字是“1”时将数字和括号省略,即KNO3
第四步:用化合价原则检查:(+1)+(-1)=0
因此KNO3就是硝酸钾的化学式.
(2)由图可以看出:图中共有核内质子数为12、17、18的三种原子,它们分别属于三种元素.
由图可以看出:选项B中核内质子数为12,核外电子数为10,核内质子数>核外电子数,因此选项B中的原子为阳离子;核电荷数为12的元素是镁元素,元素符号为Mg;由图还可以看出该镁原子失去了两个电子,因而带有了两个单位的正电荷.因此选项B是带有两个单位正电荷的镁离子,其离子符号为Mg2+.
根据元素周期表中元素的排列规律可知选项A所示的元素位于元素周期表的第三周期.
故答案为:
(1)Cu;K2O;KNO3.
(2)3;Mg2+;3.
化合价不是零的金属元素只有+1价的钾元素,它形成的氧化物是氧化钾.其化学式的书写步骤如下:
第一步:写出元素符号,氧元素符号在右,碳元素符号在左:KO
第二步:标注元素的化合价:
| +1 |
| K |
| -2 |
| O |
第三步:化合价的绝对值交叉写在元素符号的右下角:K2O
第四步:用化合价原则检查:(+1)×2+(-2)=0
因此K2O就是钾的氧化物的化学式.
所提供的元素能形成的复合肥是硝酸钾.硝酸钾由+1价的钾元素和-1价的硝酸根构成,其化学式的书写步骤如下:
第一步:写出元素符号或原子团,正价元素或原子团的符号在左,负价元素或原子团的符号在右:KNO3
第二步:标注元素的化合价:
| -1 |
| K |
| -1 |
| NO3 |
第三步:化合价的绝对值交叉写在元素符号的右下角:K1(NO3)1.数字是“1”时将数字和括号省略,即KNO3
第四步:用化合价原则检查:(+1)+(-1)=0
因此KNO3就是硝酸钾的化学式.
(2)由图可以看出:图中共有核内质子数为12、17、18的三种原子,它们分别属于三种元素.
由图可以看出:选项B中核内质子数为12,核外电子数为10,核内质子数>核外电子数,因此选项B中的原子为阳离子;核电荷数为12的元素是镁元素,元素符号为Mg;由图还可以看出该镁原子失去了两个电子,因而带有了两个单位的正电荷.因此选项B是带有两个单位正电荷的镁离子,其离子符号为Mg2+.
根据元素周期表中元素的排列规律可知选项A所示的元素位于元素周期表的第三周期.
故答案为:
(1)Cu;K2O;KNO3.
(2)3;Mg2+;3.
点评:本题主要考查元素符号、离子符号、化学式的书写和化合价的应用,难度较大.

练习册系列答案
 轻松暑假总复习系列答案
轻松暑假总复习系列答案
相关题目

 五种元素中,选择适当的元素,按要求写出相应物质的化学式:单质;金属氧化物;可作为复合肥料的盐(每空只填一种物质).
五种元素中,选择适当的元素,按要求写出相应物质的化学式:单质;金属氧化物;可作为复合肥料的盐(每空只填一种物质).