题目内容
【题目】实验室用如图装置进行碳酸钠的性质实验,烧杯A中是澄清石灰水并滴加了酚酞,C中是石灰乳.实验开始前,称取10.6g纯碱置于B中,关闭开关K1打开K2 , 并加入一定量的稀硫酸. 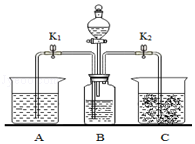
①烧杯C中并没有明显现象,为了证明B中的确产生了CO2 , 现将C中液体进行固液分离,该分离操作除烧杯外,还需用到的玻璃仪器有(写名称).过滤后滤液能使酚酞试液变红,则滤液中的主要溶质是 , 该现象(填写“能”或“不能”)说明产生了CO2 .
②上述过滤后的滤渣可能存在Ca(OH)2和CaCO3 . 某同学为证明该两种物质同时存在,在一支试管中取少量样品,经过两个步骤完成了检验.若所有检验实验均在该支试管中进行,请完成实验报告:
实验步骤 | 所用的试剂或检验方法 | 结 论 |
步骤一 | 证明存在 | |
步骤二 | 证明存在 |
③实验一段时间后,关闭开关K2打开K1 , 见到B中液体将会压入到烧杯A中,实验中可能见到不同的现象,请完成下表:
预测的反应现象 | B中反应后,溶液中溶质的化学式 | 烧杯A中发生的主要反应的化学方程式 |
A中溶液产生大量的白色沉淀产生,红色不褪去. | ||
A中溶液并没有大量的白色沉淀产生,红色褪去. |
【答案】漏斗、玻璃棒;Ca(OH)2;不能;取样于试管中,加入适量的水,滴加酚酞试液,溶液变红;氢氧化钙;继续滴加足量盐酸,有气泡产生;碳酸钙;Na2CO3、Na2SO4;Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;H2SO4、Na2SO4;H2SO4+Ca(OH)2═CaSO4+2H2O
【解析】解:①将C中液体进行固液分离可以进行过滤,过滤除烧杯外,还需用到的玻璃仪器有漏斗、玻璃棒; 过滤后滤液能使酚酞试液变红,则滤液中的主要溶质是 Ca(OH)2 , 该现象不能说明产生了二氧化碳,这是因为滤液能使酚酞试液变红,说明滤液中含有氢氧化钙,不能说明是否含有碳酸钙.
故填:漏斗、玻璃棒;Ca(OH)2;不能.②步骤一:取样于试管中,加入适量的水,滴加酚酞试液,溶液变红,说明样品中含有氢氧化钙;
步骤二:继续滴加足量盐酸,有气泡产生,说明样品中含有碳酸钙,实验报告如下表所示:
实验步骤 | 所用的试剂或检验方法 | 结 论 |
步骤一 | 取样于试管中,加入适量的水,滴加酚酞试液,溶液变红 | 证明氢氧化钙存在 |
步骤二 | 继续滴加足量盐酸,有气泡产生 | 证明碳酸钙存在 |
③A中溶液产生大量的白色沉淀产生,红色不褪去,说明B中反应后,溶液中的溶质是碳酸钠和硫酸钠,即硫酸和碳酸钠反应时碳酸钠过量,碳酸钠和氢氧化钙反应生成白色沉淀碳酸钙和氢氧化钠;
A中溶液并没有大量的白色沉淀产生,红色褪去,说明B中反应后,溶液中的溶质是硫酸和硫酸钠,即硫酸和碳酸钠反应时硫酸过量,稀硫酸和氢氧化钙反应生成硫酸钙和水,实验报告如下表所示:
预测的反应现象 | B中反应后,溶液中溶质的化学式 | 烧杯A中发生的主要反应的化学方程式 |
A中溶液产生大量的白色沉淀产生,红色不褪去 | Na2CO3、Na2SO4 | Na2CO3+Ca(OH)2═CaCO3↓+2NaOH |
A中溶液并没有大量的白色沉淀产生,红色褪去 | H2SO4、Na2SO4 | H2SO4+Ca(OH)2═CaSO4+2H2O |
【考点精析】掌握过滤操作的注意事项和书写化学方程式、文字表达式、电离方程式是解答本题的根本,需要知道过滤操作注意事项:“一贴”“二低”“三靠;过滤后,滤液仍然浑浊的可能原因有:①承接滤液的烧杯不干净②倾倒液体时液面高于滤纸边缘③滤纸破损;注意:a、配平 b、条件 c、箭号.