题目内容
某校科学兴趣小组为测定某样品中氯化铵的质量分数,将6 g样品溶于18 g水后,再加入7.6 g氢氧化钠浓溶液共热,两者恰好完全反应(样品中的杂质不与氢氧化钠反应,也不溶于水,氯化铵与氢氧化钠的反应方程式为NH4Cl+NaOH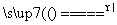 NaCl+H2O+NH3↑)。把产生的所有NH3用足量的硫酸溶液完全吸收,同时测量120 s内硫酸溶液增加的质量,结果如下表所示。
NaCl+H2O+NH3↑)。把产生的所有NH3用足量的硫酸溶液完全吸收,同时测量120 s内硫酸溶液增加的质量,结果如下表所示。
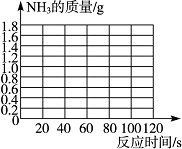
| 时间/s | 0 | 20 | 30 | 40 | 60 | 80 | 100 | 120 |
| 硫酸溶液增 加的质量/g |
| 0.7 | 1.0 | 1.2 | 1.5 | 1.6 | 1.7 | 1.7 |
试回答下列问题:
(1)请在下图中画出产生气体的质量随反应时间变化的关系曲线;
(2)样品中氯化铵的质量分数为______;
(3)求反应后所得氯化钠溶液的溶质质量分数(不考虑反应过程中的损失)。
答案:(1)如下图所示:

(2)89.2%
(3)解:设样品中NH4Cl的质量为x,生成的氯化钠质量为y。
NH4Cl+NaOH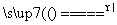 NaCl+H2O+NH3↑
NaCl+H2O+NH3↑
53.5 58.5 17
x y 1.7 g
 =
= =
=
x=5.35 g y=5.85 g
反应后溶液质量=5.35 g+18 g+7.6 g-1.7 g=29.25 g
则氯化钠溶液的溶质质量分数=5.85 g÷29.25 g×100%=20%。
答:氯化钠溶液的溶质质量分数为20%。

练习册系列答案
相关题目
 0
0