题目内容
欲确定某碳酸钠样品(含有少量硫酸钠)中其碳酸钠的质量分数,可进行如下实验:称取样品ag,加水溶解,在该溶液中加入过量的盐酸使溶液呈酸性,再加入过量氯化钡溶液,过滤、洗涤沉淀,并将沉淀烘干,称量沉淀为bg.请回答:
(1)溶液用盐酸酸化的原因是______;
(2)需要加入过量氯化钡溶液的原因是______;
(3)检验氯化钡是否加入过量的方法是______;
(4)计算样品中含Na2CO3质量分数的表达式是______.
【答案】分析:(1)碳酸钠可以和氯化钡反应生成白色沉淀,但是该白色沉淀可以溶于酸,可以据此解答;
(2)加入过量的氯化钡可以使样品中的硫酸根离子全部转化为沉淀而使就算结果更准确;
(3)如果氯化钡过量滤液中则会含有钡离子,所以可以据此来解答该题;
(4)根据化学方程式求出硫酸钠的质量进而可以表示出碳酸钠的质量分数.
解答:解:(1)碳酸钠和硫酸钠都可以和氯化钡溶液反应生成白色的沉淀,但是碳酸钡可以溶于稀盐酸,而硫酸钡不溶于酸,即在酸性的环境中不能形成碳酸钡沉淀,所以为了防止碳酸根离子干扰实验现象,要加入稀盐酸来酸化;
(2)加入过量的碳酸钡为了将溶液中的硫酸根离子全部转化为沉淀,以使结果更准确;
(3)如果加入的氯化钡是过量的则在滤液中依然存在着钡离子,那么若要验证滤液中是否含有钡离子,可以向滤液中加入硫酸钠,看是否能够产生沉淀,如果产生了沉淀,说明氯化钡是过量的,如果没有白色沉淀产生则说明氯化钡不是过量的;
(4)根据题意可知发生的反应为硫酸钠和氯化钡的反应,同时生成硫酸钡的质量为bg,所以可以据此求出硫酸钠的质量,进而求出碳酸钠的质量,然后得出样品中碳酸钠的质量分数;
设硫酸钠的质量为x
BaCl2+Na2SO4═2NaCl+BaSO4↓
142 233
x bg
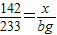
解得:x= g
g
所以碳酸钠的质量分数可以表示为: ×100%.
×100%.
故答案为:(1)为了防止碳酸根离子干扰实验现象;
(2)使硫酸根离子沉淀完全,得到更准确的结果;
(3)向滤液中加入硫酸钠,如果产生沉淀则说明氯化钡是过量的,反之则不是过量的;
(4) ×100%.
×100%.
点评:熟练掌握常见的碳酸盐和硫酸盐的化学性质,知道可溶性的碳酸盐和硫酸盐都能够和钡离子生成白色的沉淀,但是硫酸钡不溶于盐酸和硝酸,而碳酸钡可以溶于盐酸和硝酸,所以在鉴别硫酸根时要用酸化的钡盐来防止碳酸根离子的干扰.
(2)加入过量的氯化钡可以使样品中的硫酸根离子全部转化为沉淀而使就算结果更准确;
(3)如果氯化钡过量滤液中则会含有钡离子,所以可以据此来解答该题;
(4)根据化学方程式求出硫酸钠的质量进而可以表示出碳酸钠的质量分数.
解答:解:(1)碳酸钠和硫酸钠都可以和氯化钡溶液反应生成白色的沉淀,但是碳酸钡可以溶于稀盐酸,而硫酸钡不溶于酸,即在酸性的环境中不能形成碳酸钡沉淀,所以为了防止碳酸根离子干扰实验现象,要加入稀盐酸来酸化;
(2)加入过量的碳酸钡为了将溶液中的硫酸根离子全部转化为沉淀,以使结果更准确;
(3)如果加入的氯化钡是过量的则在滤液中依然存在着钡离子,那么若要验证滤液中是否含有钡离子,可以向滤液中加入硫酸钠,看是否能够产生沉淀,如果产生了沉淀,说明氯化钡是过量的,如果没有白色沉淀产生则说明氯化钡不是过量的;
(4)根据题意可知发生的反应为硫酸钠和氯化钡的反应,同时生成硫酸钡的质量为bg,所以可以据此求出硫酸钠的质量,进而求出碳酸钠的质量,然后得出样品中碳酸钠的质量分数;
设硫酸钠的质量为x
BaCl2+Na2SO4═2NaCl+BaSO4↓
142 233
x bg
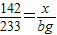
解得:x=
 g
g所以碳酸钠的质量分数可以表示为:
 ×100%.
×100%.故答案为:(1)为了防止碳酸根离子干扰实验现象;
(2)使硫酸根离子沉淀完全,得到更准确的结果;
(3)向滤液中加入硫酸钠,如果产生沉淀则说明氯化钡是过量的,反之则不是过量的;
(4)
 ×100%.
×100%.点评:熟练掌握常见的碳酸盐和硫酸盐的化学性质,知道可溶性的碳酸盐和硫酸盐都能够和钡离子生成白色的沉淀,但是硫酸钡不溶于盐酸和硝酸,而碳酸钡可以溶于盐酸和硝酸,所以在鉴别硫酸根时要用酸化的钡盐来防止碳酸根离子的干扰.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目