题目内容
【题目】某同学在学习酸的性质时做了如下实验:该同学向盛有Na2CO3溶液的试管中滴加稀盐酸至过量,发现开始没有气泡,过一会才有气泡冒出。该同学翻阅资料发现:少量盐酸与Na2CO3溶液反应生成NaHCO3和NaCl。
(1)该同学向含Na2CO310.6g的溶液中滴加质量分数为18.25%的稀盐酸,产生气体2.2g,则滴加该盐酸的质量为_________g。
(2)该同学又向200gNa2CO3和NaHCO3混合溶溶液中滴加质量分数为18.25%的稀盐酸至过量,产生气体的量与加入盐酸的质量关系如图。
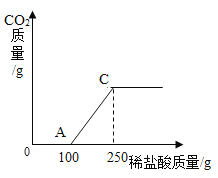
①写出AC段发生反应的化学方程式__________。
②该混合液中Na2CO3的质量分数为________;NaHCO3的质量分数为__________。
【答案】30 ![]() 26.5% 10.5%
26.5% 10.5%
【解析】
(1)解:设与含Na2CO310.6g的溶液反应的氯化氢的质量为X。

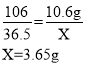
设产生气体2.2g消耗氯化氢的质量为Y。
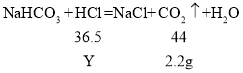
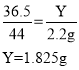
滴加该盐酸的质量为![]() 。
。
(2)①依据题目图示分析,AC段有二氧化碳气体产生,发生反应的化学方程式![]() 。
。
②解:设该混合液中Na2CO3的质量为n,生成NaHCO3的质量为m。
与混合液中Na2CO3反应的氯化氢的质量为![]() 。
。
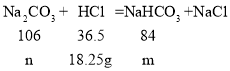
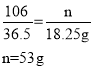
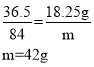
该混合液中Na2CO3的质量分数为![]() 。
。
设与盐酸反应的NaHCO3的质量为Z。与NaHCO3反应的氯化氢的质量为![]()
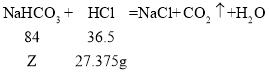
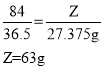
该混合液中NaHCO3的质量分数为:
![]()
答:该混合液中Na2CO3的质量分数为26.5%;NaHCO3的质量分数为10.5%。

练习册系列答案
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案
相关题目