题目内容
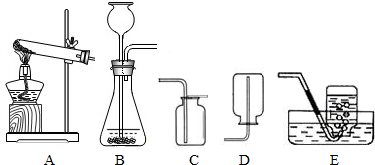
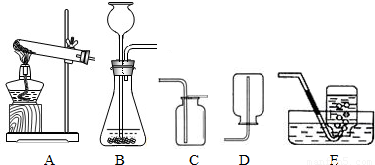
(1)在实验室制取二氧化碳的实验中,将产生的气体通入到新制的澄清石灰水中,发现澄清石灰水不变浑浊,其原因可能是
(2)测得某溶液中含有Na+、S
、M
、N
四种离子,其中离子个数比为Na+:M
:N
=4:5:8.若设有Na+个数为4n时,则S
的个数为
(3)家用煤炉使用的燃料是煤,把煤做成蜂窝状的目的是
(4)日常生活中,用于保护钢铁制品所使用的“银粉”实际上是金属
(5)在盛有200克溶质质量分数为9.8%稀硫酸的烧杯中,加入一定质量的氯化钡溶液产生了23.3克的沉淀,静置,再加入足量的金属镁,则产生氢气的质量是
制取二氧化碳时所用的盐酸浓度较大
制取二氧化碳时所用的盐酸浓度较大
;(2)测得某溶液中含有Na+、S
| O | 2- 4 |
| g | 2+ |
| O | - 3 |
| g | 2+ |
| O | - 3 |
| O | 2- 4 |
3n
3n
个.(3)家用煤炉使用的燃料是煤,把煤做成蜂窝状的目的是
增大煤与氧气的接触面积,使煤燃烧更加充分
增大煤与氧气的接触面积,使煤燃烧更加充分
,在做蜂窝煤时,往往向煤中添加一些生石灰的原因是除去煤燃烧产生的二氧化硫
除去煤燃烧产生的二氧化硫
.(4)日常生活中,用于保护钢铁制品所使用的“银粉”实际上是金属
铝
铝
的粉末;温度计中填充的金属是汞
汞
.(5)在盛有200克溶质质量分数为9.8%稀硫酸的烧杯中,加入一定质量的氯化钡溶液产生了23.3克的沉淀,静置,再加入足量的金属镁,则产生氢气的质量是
0.4
0.4
克.分析:(1)浓盐酸易挥发,二氧化碳能使澄清的石灰水变浑浊;
(2)溶液中,阳离子所带正电荷总数等于阴离子所带负电荷总数;
(3)增大可燃物与氧气的接触面积,或增大氧气的浓度,都能够促进可燃物燃烧,高温条件下,氧化钙能和二氧化硫反应生成亚硫酸钙;
(4)铝的化学性质比较活泼,通常情况下,能被空气中的氧气氧化,从而在表面形成一层保护膜,对里面的物质起到保护作用,汞可以用作温度计中的液体;
(5)根据已知量和反应的化学方程式,可以进行相关方面的计算.
(2)溶液中,阳离子所带正电荷总数等于阴离子所带负电荷总数;
(3)增大可燃物与氧气的接触面积,或增大氧气的浓度,都能够促进可燃物燃烧,高温条件下,氧化钙能和二氧化硫反应生成亚硫酸钙;
(4)铝的化学性质比较活泼,通常情况下,能被空气中的氧气氧化,从而在表面形成一层保护膜,对里面的物质起到保护作用,汞可以用作温度计中的液体;
(5)根据已知量和反应的化学方程式,可以进行相关方面的计算.
解答:解:(1)制取二氧化碳时,如果用的盐酸浓度较大,挥发性增强,挥发出的氯化氢气体随着二氧化碳进入石灰水中,能和石灰水中的氢氧化钙反应生成氯化钙和水,从而导致澄清的石灰水不变浑浊.
故填:制取二氧化碳时所用的盐酸浓度较大.
(2)Na+个数为4n时,Mg2+个数为5n,NO3-个数为8n,则SO42-个数为:(4n+5n×2-8n)÷2=3n,
故填:3n.
(3)把煤做成蜂窝状,能够增大煤与氧气的接触面积,从而促进煤的燃烧;
煤中含有硫,燃烧时能够生成二氧化硫,高温条件下二氧化硫能和生石灰反应生成亚硫酸钙,从而除去二氧化硫,防止污染环境.
故填:增大煤与氧气的接触面积,使煤燃烧更加充分;除去煤燃烧产生的二氧化硫.
(4)钢铁制品涂上一层铝粉时,铝粉能被空气中的氧气氧化成一层致密的氧化物薄膜,对里面的物质起到保护作用;
温度计中填充的金属是汞.
故填:铝;汞.
(5)解:设加入足量的金属镁时,产生氢气的质量为x,
稀硫酸和氯化钡反应生成硫酸钡沉淀和盐酸,不管稀硫酸和氯化钡是否恰好完全反应,最后和镁反应的氢离子都来自于稀硫酸中的氢离子,
Mg+H2SO4═MgSO4+H2↑,
98 2
200g×9.8% x
=
,
x=0.4g,
故填:0.4.
故填:制取二氧化碳时所用的盐酸浓度较大.
(2)Na+个数为4n时,Mg2+个数为5n,NO3-个数为8n,则SO42-个数为:(4n+5n×2-8n)÷2=3n,
故填:3n.
(3)把煤做成蜂窝状,能够增大煤与氧气的接触面积,从而促进煤的燃烧;
煤中含有硫,燃烧时能够生成二氧化硫,高温条件下二氧化硫能和生石灰反应生成亚硫酸钙,从而除去二氧化硫,防止污染环境.
故填:增大煤与氧气的接触面积,使煤燃烧更加充分;除去煤燃烧产生的二氧化硫.
(4)钢铁制品涂上一层铝粉时,铝粉能被空气中的氧气氧化成一层致密的氧化物薄膜,对里面的物质起到保护作用;
温度计中填充的金属是汞.
故填:铝;汞.
(5)解:设加入足量的金属镁时,产生氢气的质量为x,
稀硫酸和氯化钡反应生成硫酸钡沉淀和盐酸,不管稀硫酸和氯化钡是否恰好完全反应,最后和镁反应的氢离子都来自于稀硫酸中的氢离子,
Mg+H2SO4═MgSO4+H2↑,
98 2
200g×9.8% x
| 98 |
| 2 |
| 200g×9.8% |
| x |
x=0.4g,
故填:0.4.
点评:稀硫酸和稀盐酸和镁反应都能够生成氢气,因此根据稀硫酸的质量计算生成氢气的质量比较简单,可以化繁为简.

练习册系列答案
相关题目