��Ŀ����
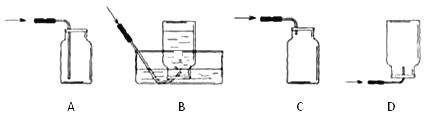
����Ŀ����ͼΪijͬѧ������ʵ�鼰����

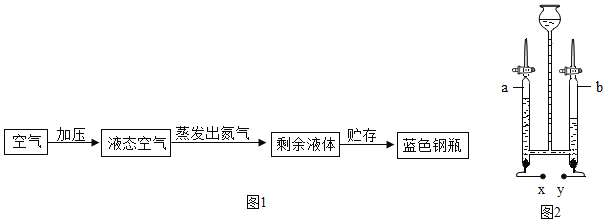
��1��ʵ��1������Ӧ�Ļ�ѧ����ʽΪ_________��
��2��ʵ��2����Ca(HCO3)2��ʵ��3������Ӧ�Ļ�ѧ����ʽΪ________����ʵ��˵��CaCO3��Ca(HCO3)2���ȶ���__________��ѡ�ǿ������������
��3��ij����Ӳˮ�����н϶�Ŀ�����Ca(HCO3)2��Mg(HCO3)2��
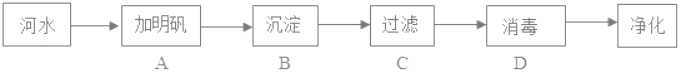
�������г���__________������Ӳˮ����ˮ��
�����Ӳˮ�ɽ���ˮ��Ӳ�ȣ�ͬʱ���������Ի�������A��
�����룩����A�г�CaCO3�⣬�����У�
����1��ֻ��MgCO3 ����2��ֻ��Mg(OH)2 ����3��MgCO3��Mg(OH)2
�����ϣ���MgCO3��ϡ����ķ�Ӧ��CaCO3���ƣ�д��MgCO3��ϡ���ᷴӦ�Ļ�ѧ����ʽ____________��
��Mg(OH)2��ϡ���ᷴӦ�����Ȼ�þ��ˮ
��ʵ�飩ȡ10.0 g����Ĺ���A������������ϡ�����ַ�Ӧ������4.4 gCO2���塣
�����ۣ��ٲ���1��2���������жϲ���1�����������_________��
�ڲ���3��ȷ������A��MgCO3��Mg(OH)2����������________��
���𰸡�CO2+Ca��OH��2�TCaCO3��+H2O Ca��HCO3��2![]() CaCO3��+CO2��+H2O ǿ ����ˮ MgCO3+2HCl=MgCl2+H2O+CO2�� ��ֻ��MgCO3�������ɵ�CO2����4.4g 21��4
CaCO3��+CO2��+H2O ǿ ����ˮ MgCO3+2HCl=MgCl2+H2O+CO2�� ��ֻ��MgCO3�������ɵ�CO2����4.4g 21��4
��������
��1��������̼���������Ʒ�Ӧ����̼��ư�ɫ������ˮ����Ӧ�Ļ�ѧ����ʽΪ��CO2+Ca��OH��2�TCaCO3��+H2O��
��2���ڼ��ȵ������£�̼����Ʒֽ�Ϊ̼��ơ�ˮ�Ͷ�����̼����Ӧ�Ļ�ѧ����ʽΪ��Ca��HCO3��2![]() CaCO3��+CO2��+H2O����˵��CaCO3��Ca��HCO3��2���ȶ���ǿ��
CaCO3��+CO2��+H2O����˵��CaCO3��Ca��HCO3��2���ȶ���ǿ��
��3��������Ӳˮ����ˮ�ķ����ǣ��÷���ˮ���������ˮ����ĭ�������ˮ����ĭ�ٵ���Ӳˮ��
[����]��̼��þ�����ᷴӦ�����Ȼ�þ��������̼��ˮ����Ӧ�Ļ�ѧ����ʽΪ��MgCO3+2HCl=MgCl2+H2O+CO2����
[����]�ɻ�ѧ����ʽ��
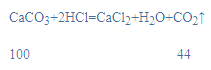
��
��֪��10.0g̼��������������ᷴӦ���ɶ�����̼������Ϊ4.4g��10.0g̼��þ��������ϡ���ᷴӦ���ɶ�����̼����������4.4g��������þ�����ᷴӦ�������ɶ�����̼��
����ֻ��MgCO3�������ɵ�CO2����4.4g�����Բ���1����
���������3��ȷ��10.0g̼��ƺ�ϡ������ȫ��Ӧ����4.4g������̼����˹���A��MgCO3��Mg��OH��2���������ǣ�8.4g����10.0g-8.4g��=21��4��