题目内容
【题目】某公司生产出的纯碱产品中经检测只含有氯化钠杂质。为测定产品中碳酸钠的质量分数,20℃时,称取该产品样品26.5g,加入到盛有一定质量稀盐酸的烧杯中,碳酸钠与稀盐酸恰好完全反应,气体完全逸出,得到不饱和NaCl溶液。反应过程用精密仪器测得烧杯内混合物的质量(m)与反应时间(t)关系如下图所示。

求:(1)计算碳酸钠中各元素的质量比:Na:C:O= 。
(2)碳酸钠的相对分子质量为: 。
(3)生成CO2的质量。
(4)该纯碱样品中Na2CO3的质量分数。
【答案】(1)Na:C:O=23:6:24 (2)106 (3)8.8克(4)80%
【解析】
试题分析:Na:C:O=23×2:12×1:3×16=23:6:24 ;碳酸钠的相对分子质量为=23×2+12×1+3×16=106 ;根据质量守恒定律可以知道:生成二氧化碳的质量为172.5g-163.7 g = 8.8 g
设:样品中碳酸钠的质量为x
Na2CO3 + 2HCl == 2NaCl + CO2 ↑ + H2O
106 44
x 8.8g
列比例式得:106:X=44:8.8克 求得X=21.2克
则该纯碱样品中碳酸钠的质量分数为21.2克/26.5克×100%=80 %

【题目】铝元素与人类关系密切。
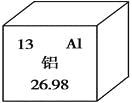
(1)铝是地壳中含量最高的________元素。
(2)元素周期表中铝元素的信息如图所示,其原子的核外电子数为________。
(3)铝元素在自然界中主要以Al2O3存在,Al2O3属于________(填字母序号)。
A.单质 | B.氧化物 | C.碱 | D.盐 |
(4)工业用电解熔融Al2O3的方法冶炼铝,化学方程式为2Al2O3![]() 4Al+3O2↑,该反应属于基本反应类型中的____反应。在Al2O3中铝的化合价为 。
4Al+3O2↑,该反应属于基本反应类型中的____反应。在Al2O3中铝的化合价为 。
(5)铝可制成蒸锅,主要利用铝的延展性和____性。