题目内容
【题目】碳是形成化合物种类最多的元素,含碳物质是中学化学研究的重要内容.
(1)“低碳生活”倡导低能量、低消耗,主要是为了减少(填化学式)的排放量.
(2)如图1为元素周期表中的一格,下列说法不正确的是(填标号).
A.碳元素属于非金属元素
B.碳原子核内质子数为6
C.碳元素的原子结构示意图为 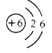
D.碳的相对原子质量为12.01
(3)利用图2装置可做CO还原Fe2O3 , 的实验,并检验该反应生成的气体产物.已知由A装置制取的CO气体中混有少量的CO2 . (提示:二氧化碳可以与氢氧化钠溶液反应) 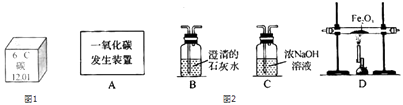
①CO与Fe2O3反应的化学方程式为 .
②气体通过装置的顺序是A→(装置不能重复使用).
③请仿照CO2与澄清石灰水的反应原理,写出CO2与氢氧化钠溶液反应的化学方程式 .
④从环保角度考虑,对以上装置的改进措施是 .
(4)称取12.5g石灰石(主要成分是CaCO3 , 杂质不参加反应)放入烧杯中,向其中加入50g稀盐酸,二者恰好完全反应.反应结束后称量烧杯中剩余物质的总质量为58.1g(不包括烧杯的质量,且气体的溶解忽略不计).试计算石灰石中杂质的质量分数.
【答案】
(1)CO2
(2)C
(3)3CO+Fe2O3 ![]() 2Fe+3CO2;CDB;CO2+2NaOH=Na2CO3+H2O;B装置连上集气瓶收集剩余的一氧化碳
2Fe+3CO2;CDB;CO2+2NaOH=Na2CO3+H2O;B装置连上集气瓶收集剩余的一氧化碳
(4)解:据质量守恒定律可知,生成的二氧化碳的质量为12.5g+50g﹣58.1g=4.4g.
设12.5 g 石灰石样品中含CaCO3的质量为x
CaCO 3+2HCl═CaCl2+H2O+ | CO2↑ |
100 | 44 |
x | 4.4 g |
![]() =
= ![]()
x=10 g
杂质的质量分数= ![]() ×100%=20%
×100%=20%
【解析】解:(1)“低碳生活”倡导低能量、低消耗,主要是为了减少CO2 (填化学式,不得填写为名称,否则不得分,另外不要受遇到元素名称就说是元素,而不具体考虑)的排放量.(2)如图1为元素周期表中的一格,对应的是碳元素的有关信息,其原子的核外的电子排布为2,4,所以C是错误的.(3)利用图2装置可做CO还原Fe2O3实验,并检验该反应生成的气体产物.已知由A装置制取的CO气体中混有少量的CO2 . 由于一氧化碳中混有二氧化碳,所以要先排除二氧化碳的干扰,而“提示:二氧化碳可以与氢氧化钠溶液反应“,所以可以用氢氧化钠溶液吸收除去二氧化碳.然后一氧化碳和氧化铁反应,生成气体通入到石灰水中检验二氧化碳的生成.本题更准确的方法是A→C(吸收二氧化碳)→B(证明二氧化碳吸收干净)→D→B,但是题目默认装置不能重复使用,意思只要吸收那就吸收干净了.所以是A→CDB.①CO与Fe2O3反应的化学方程式为3CO+Fe2O3 ![]() 2Fe+3CO2 . ②气体通过装置的顺序是A→CDB(装置不能重复使用).③O2与澄清石灰水生成碳酸钙和水,所以CO2与氢氧化钠溶液反应生成碳酸钠和水,对应化学方程式 CO2+2NaOH=Na2CO3+H2O.④从环保角度考虑,对以上装置的改进措施是 B装置连上集气瓶收集剩余的一氧化碳.(4)所以答案是:(1)CO2;(2)C;(3)①3CO+Fe2O3
2Fe+3CO2 . ②气体通过装置的顺序是A→CDB(装置不能重复使用).③O2与澄清石灰水生成碳酸钙和水,所以CO2与氢氧化钠溶液反应生成碳酸钠和水,对应化学方程式 CO2+2NaOH=Na2CO3+H2O.④从环保角度考虑,对以上装置的改进措施是 B装置连上集气瓶收集剩余的一氧化碳.(4)所以答案是:(1)CO2;(2)C;(3)①3CO+Fe2O3 ![]() 2Fe+3CO2②CDB;③CO2+2NaOH=Na2CO3+H2O.④B装置连上集气瓶收集剩余的一氧化碳.(4)据质量守恒定律可知,生成的二氧化碳的质量为12.5g+50g﹣58.1g=4.4g.
2Fe+3CO2②CDB;③CO2+2NaOH=Na2CO3+H2O.④B装置连上集气瓶收集剩余的一氧化碳.(4)据质量守恒定律可知,生成的二氧化碳的质量为12.5g+50g﹣58.1g=4.4g.
CaCO 3+2HCl═CaCl2+H2O+ | CO2↑ |
100 | 44 |
x | 4.4 g |
![]() =
= ![]()
x=10 g
杂质的质量分数= ![]() ×100%=20%
×100%=20%
【考点精析】解答此题的关键在于理解二氧化碳对环境的影响的相关知识,掌握二氧化碳多环境的影响:过多排放引起温室效应,以及对一氧化碳还原氧化铁的理解,了解原理:在高温下,利用焦炭与氧气反应生成的一氧化碳把铁从铁矿石里还原出来.