题目内容
如右图所示,在密闭容器内的两只烧杯中,A杯中加有50ml水,有一粒绿豆大的白磷浸没在水中,B烧杯中含有一粒绿豆大的白磷.(1)当恒温箱的温度由25℃逐渐上升至60℃,A、B烧杯中白磷出现的变化(白磷着火点为40℃):A烧杯 ;B烧杯 .
(2)由上述实验可知,可燃物燃烧的条件是 和 .
(3)平时实验室应将少量白磷保存在 中.
(4)写出磷燃烧的化学方程式 .

【答案】分析:燃烧需要同时满足三个条件:①物质具有可燃性 ②与氧气接触 ③温度达到可燃物的着火点.
解答:解:(1)当恒温箱的温度由25℃逐渐上升至60℃,B烧杯中白磷达到了着火点,并且有充足的氧气,白磷燃烧;
A烧杯中白磷浸没在水中,与氧气不接触,不能燃烧;
(2)由上述实验可知,可燃物燃烧的条件是:温度达到着火点,有充足的氧气;
(3)白磷在空气中容易发生缓慢氧化,所以常常将白磷浸没在冷水中保存,其主要目的是防止白磷与空气中的氧气接触.
(4)磷燃烧生成五氧化二磷,化学方程式为:4P+5O2 2P2O5.
2P2O5.
故答案为:(1)无明显现象(或白磷不燃烧);白磷燃烧;
(2)温度达到着火点,有充足的氧气;
(3)水;
(4)4P+5O2 2P2O5.
2P2O5.
点评:该题重点考查学生根据燃烧的条件进行分析解题的能力,并将知识灵活应用.
解答:解:(1)当恒温箱的温度由25℃逐渐上升至60℃,B烧杯中白磷达到了着火点,并且有充足的氧气,白磷燃烧;
A烧杯中白磷浸没在水中,与氧气不接触,不能燃烧;
(2)由上述实验可知,可燃物燃烧的条件是:温度达到着火点,有充足的氧气;
(3)白磷在空气中容易发生缓慢氧化,所以常常将白磷浸没在冷水中保存,其主要目的是防止白磷与空气中的氧气接触.
(4)磷燃烧生成五氧化二磷,化学方程式为:4P+5O2
 2P2O5.
2P2O5.故答案为:(1)无明显现象(或白磷不燃烧);白磷燃烧;
(2)温度达到着火点,有充足的氧气;
(3)水;
(4)4P+5O2
 2P2O5.
2P2O5.点评:该题重点考查学生根据燃烧的条件进行分析解题的能力,并将知识灵活应用.

练习册系列答案
 寒假学与练系列答案
寒假学与练系列答案
相关题目
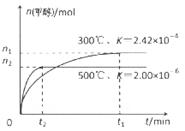 (1)用CO合成甲醇的反应为:CO(g)+2H2(g)
(1)用CO合成甲醇的反应为:CO(g)+2H2(g)  CH3OH (g)
CH3OH (g) CH3OH+H2O。
CH3OH+H2O。
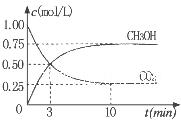 ②为探究用CO2生产燃料甲醇的反应原理,现进行如下实验:在一恒温恒容密闭容器中,充入1molCO2 和3molH2,进行上述反应。测得CO2。
②为探究用CO2生产燃料甲醇的反应原理,现进行如下实验:在一恒温恒容密闭容器中,充入1molCO2 和3molH2,进行上述反应。测得CO2。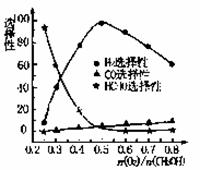 ①甲醇蒸汽重整法。主要反应为;CH3OH(g)
①甲醇蒸汽重整法。主要反应为;CH3OH(g)