题目内容
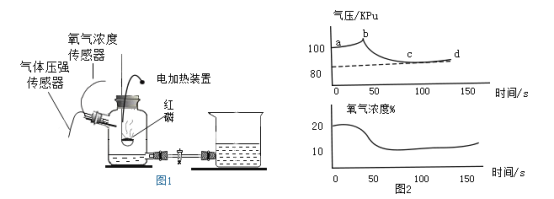
【题目】某化学兴趣小组为探究镁、铁、锌、铜的金属活动性顺序,设计了如图所示 的三个实验(其中金属均已打磨,且形状、大小相同;所用盐酸的溶质质量分数、用量也相同)。下列判断错误的是( )
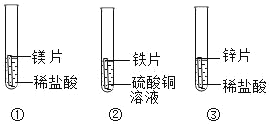
A.通过实验①和③的反应剧烈程度,可以判断出镁和锌的金属活动性强弱
B.在上述三个实验基础上再增加一个铁和稀盐酸的实验,则可判断出四种金属 的活动顺序
C.通过上述三个实验,能判断出四种金属的活动性顺序
D.通过实验②的反应现象,可以判断出铜和铁的金属活动性强弱
【答案】C
【解析】
A、金属的活动性越强,与酸反应的速率越快,通过实验①和③的 反应剧烈程度,可以判断出铁和镁的金属活动性强弱,故A选项正确,不合题意;
B、若增加一个铁和稀盐酸的实验,根据产生气泡的速率快慢,能得出活动性镁>锌>铁,由实验②,铁片的表面覆盖一层红色物质,说明活动性铁>铜,可得 金属活动性镁>锌>铁>铜,故B选项正确,不合题意;
C、根据实验①和③,均能产生气泡,且①产生气泡的速率快,说明镁的金属活动性比锌强,即Mg>Zn>H;由实验②,铁片的表面覆盖一层红色物质,说明活动性铁>铜,无法确定铁和锌的金属活动性,故C选项错误,符合题意;
D、位于前面的金属能把排在它后面的金属从其盐溶液中置换出来,通过实验②的反应现象,铁片的表面覆盖一层红色物质,说明活动性铁>铜,故D选项正确,不合题意;
故选:C。

 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案【题目】工业中合成SO3的反应:2SO2+O2![]() 2SO3。一定条件下,在一密闭容器内投入 SO2、O2、SO3、V2O5四种物质,在不同时刻测得各物质的质量(单位为 g)如下表所示。说法错误的是
2SO3。一定条件下,在一密闭容器内投入 SO2、O2、SO3、V2O5四种物质,在不同时刻测得各物质的质量(单位为 g)如下表所示。说法错误的是
甲 | 乙 | 丙 | 丁 | |
t1 | 100 | 5 | 80 | 5 |
t2 | 60 | 55 | a | b |
t3 | 40 | c | d | 5 |
A.丁物质一定是V2O5
B.d=15
C.丙物质是O2
D.t3时,生成乙75g
【题目】蔗糖是生活中常见的一种物质,某兴趣小组对“蔗糖的组成”进行了探究。
(作出猜想)小组同学认为绿色植物通过光合作用将二氧化碳和水转化成葡萄糖和氧气,葡萄糖进一步转化为蔗糖,故蔗糖中一定含有碳、氢元素可能含有氧元素。
(实验探究)
方案一:小明将蔗糖放在氧气中燃烧,检验生成物中有水和二氧化碳得出结论“蔗糖是由碳、氢、氧三种元素组成的”。小刚认为该方案不合理,实验只能说明蔗糖中一定含有______________。
方案二:用如图所示装置进行实验,实验开始先通人一会儿氮气,然后关闭弹簧夹,点燃酒精灯给蔗糖加强热。
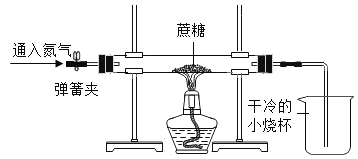
(1)先通入一会儿氮气的目的是________________。
(2)实验中酒精灯加网罩的目的是__________________。
(3)观察到_____________出现,说明蔗糖中含有氢元素和氧元素。
(4)观察到硬质玻璃管中残留有黑色固体,他猜测该黑色固体是单质碳,并继续利用如图所示装置,另选试剂进行了验证单质碳的实验。实验过程和现象如表
实验过程 | 实验现象 |
小烧杯中加入足量的澄清石灰水,往硬质玻璃管中通入氧气,点燃酒精灯 | ①硬质玻璃管中的黑色固体剧烈燃烧,发出白光; ②__________________ |
写出上述实验过程中烧杯中反应的化学方程式____________________。