题目内容
【题目】Fe,Cu.Ag是初中化学学过的三种金属,为探究它们的金属活动性顺序,将两支洁净的铁丝、铜丝分别插入足量的AgNO3溶液中.

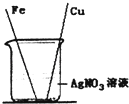
(1)一段时间后,铜丝表面出现哪些实验现象?反应后铜丝的质量与反应前相比有哪些变化(是“增大”、“减小”还是“不变”)?
(2)上述实验能否得出三种金属的活动性顺序?请说明理由.
(3)若不能得出,若要验证验证铁、铜、银三种金属的活动性顺序,可在烧杯中可加入哪种溶液(写化学式)?可观察到的哪些实验现象?
【答案】(1)有银白色物质生成、增大;(2)不能、根据铁和硝酸银溶液反应的质量关系可知,铁丝质量每减少56份质量,同时会增加216份质量的银,随着反应的进行,铁丝的质量逐渐增加,所以,反应后铁丝的质量较反应前增大,铁和铜都能置换出硝酸银溶液中的银,铁和铜的活泼性都比银强,但是,铁和铜的活泼性无法比较;(3)CuSO4、铁丝表面覆盖一层红色物质,溶液由蓝色逐渐变为浅绿色.
【解析】(1)在金属活动性顺序表中,铜排在银的前面,铜能置换出硝酸银溶液中的银,铜丝表面有银白色物质生成,故反应后铜丝的质量与反应前相比增大;
(2)根据铁和硝酸银溶液反应的质量关系可知,铁丝质量每减少56份质量,同时会增加216份质量的银,随着反应的进行,铁丝的质量逐渐增加,所以,反应后铁丝的质量较反应前增大,铁和铜都能置换出硝酸银溶液中的银,铁和铜的活泼性都比银强,但是,铁和铜的活泼性无法比较;要比较铁和铜的活泼性的大小,还要增加实验:将将铁丝放入硫酸铜溶液中.
(3)要比较铁和铜的活泼性的大小,还要增加实验:将铁丝放入硫酸铜溶液中.铁丝表面覆盖一层红色物质,溶液由蓝色逐渐变为浅绿色.

练习册系列答案
相关题目