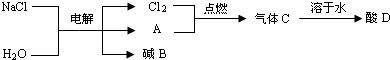
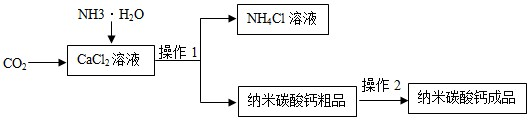
题目内容
(2012?盐城)某兴趣小组对食用纯碱和食用小苏打两种粉末进行以下探究.
[查阅资料]
[实验探究]
(1)探究两者水溶液酸碱性的差异
小明分别向等浓度的两种溶液中滴入酚酞试液,发现两者都变
(2)验证两种粉末的稳定性
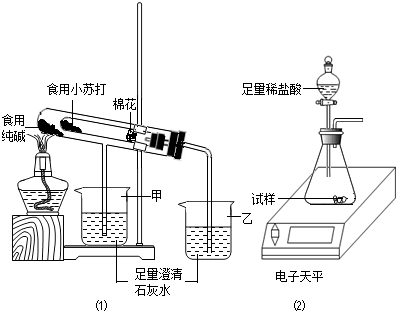
在老师的指导下,该小组按如图1装置进行实验操作,观察到
(3)测定食用纯碱粉末的纯度
取食用纯碱粉末试样,利用如图2装置进行实验测定.
数据记录如下:
①反应生成CO2的质量为
②通过计算确定食用纯碱粉末中Na2CO3的质量分数.(写出计算过程,结果保留一位小数.)
③如果测得的结果比实际纯度高,可能的原因是
[查阅资料]
| 名称 | 食用纯碱 | 食用小苏打 |
| 主要成分 | Na2CO3 | NaHCO3 |
| 酸碱性 | 水溶液显碱性 | 水溶液显碱性 |
| 热稳定性 | 受热不分解 | 270℃时完全分解为碳酸钠、二氧化碳、水 |
(1)探究两者水溶液酸碱性的差异
小明分别向等浓度的两种溶液中滴入酚酞试液,发现两者都变
红
红
色,但食用纯碱溶液中颜色更深,由此推测可能食用纯碱
食用纯碱
溶液碱性更强.小欢认为要比较两种溶液的碱性强弱,可直接用pH试纸
pH试纸
进行测定.(2)验证两种粉末的稳定性
在老师的指导下,该小组按如图1装置进行实验操作,观察到
乙
乙
(填“甲”或“乙”)烧杯中澄清石灰水变浑浊,试管中发生反应的化学方程式为2NaHCO3
Na2CO3+CO2↑+H2O
| ||
2NaHCO3
Na2CO3+CO2↑+H2O
,装置中棉花的作用是
| ||
防止加热时小苏打(或NaHCO3)粉末进入导管
防止加热时小苏打(或NaHCO3)粉末进入导管
.(3)测定食用纯碱粉末的纯度
取食用纯碱粉末试样,利用如图2装置进行实验测定.

数据记录如下:
| 称量项目 | 称量时间 | 质量/g |
| 试样 | 11.0 | |
| 装置+稀盐酸 | 160.0 | |
| 装置+稀盐酸+试样 | 反应开始后20s | 167.0 |
| 装置+稀盐酸+试样 | 反应开始后30s | 166.6 |
| 装置+稀盐酸+试样 | 反应开始后90s | 166.6 |
4.4
4.4
g.②通过计算确定食用纯碱粉末中Na2CO3的质量分数.(写出计算过程,结果保留一位小数.)
③如果测得的结果比实际纯度高,可能的原因是
稀盐酸挥发出的HCl气体随CO2气体排出,从而导致所测纯度偏大
稀盐酸挥发出的HCl气体随CO2气体排出,从而导致所测纯度偏大
.(答一种即可)分析:[实验探究]依据表中关于碳酸钠和碳酸氢钠的酸碱性及热稳定性所提供的信息分析解答(1)(2);
(3)依据反应前后质量的变化计算出生成二氧化碳的质量,根据化学方程是的计算利用二氧化碳的质量求出反应的碳酸钠的质量,进而得到食用纯碱粉末中Na2CO3的质量分数;
依据盐酸存在挥发性分析导致所求结果偏大的原因;
(3)依据反应前后质量的变化计算出生成二氧化碳的质量,根据化学方程是的计算利用二氧化碳的质量求出反应的碳酸钠的质量,进而得到食用纯碱粉末中Na2CO3的质量分数;
依据盐酸存在挥发性分析导致所求结果偏大的原因;
解答:解:(1)从表中可以看出食用纯碱和食用小苏打的水溶液均显碱性,遇酚酞均能使酚酞变红,且碱性越强颜色越红,测定溶液酸碱性强弱程度可采用pH试纸或PH计完成;
(2)由图表关于两者的热稳定性进行分析可知:食用小苏打可以加热分解生成二氧化碳,而食用纯碱不能,所以分析装置可知乙烧杯的澄清石灰水变浑浊,其分解方程式为:2NaHCO3
Na2CO3+CO2↑+H2O,装置中的棉花团的作用是:防止加热时小苏打(或NaHCO3)粉末进入导管;
(3)①由图表数据分析可知11g样品与盐酸完全反应的质量变化是(11g+160g)-166.6g=4.4g,因为此过程发生的反应是Na2CO3+2HCl=2NaCl+H2O+CO2↑,所以此质量差即是生成二氧化碳的质量;
②设生成4.4g二氧化碳时需要碳酸钠的质量是x
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 44
x 4.4g
=
x=10.6g
所以食用纯碱粉末中Na2CO3的质量分数为
×100%≈96.4%;
③通过以上计算可知如果测得的结果比实际纯度高,则是测量的二氧化碳质量比实际值偏大,可能的原因是稀盐酸挥发出的HCl气体随CO2气体排出,从而导致所测纯度偏大;
故答案为:(1)红;食用纯碱(或Na2CO3);pH试纸;
(2)乙; 2NaHCO3
Na2CO3+CO2↑+H2O;防止加热时小苏打(或NaHCO3)粉末进入导管;
(3)①4.4;②食用纯碱粉末中Na2CO3的质量分数为96.4%;③稀盐酸挥发出的HCl气体随CO2气体排出,从而导致所测纯度偏大.(或水蒸气随CO2气体排出,从而导致所测纯度偏大)
(2)由图表关于两者的热稳定性进行分析可知:食用小苏打可以加热分解生成二氧化碳,而食用纯碱不能,所以分析装置可知乙烧杯的澄清石灰水变浑浊,其分解方程式为:2NaHCO3
| ||
(3)①由图表数据分析可知11g样品与盐酸完全反应的质量变化是(11g+160g)-166.6g=4.4g,因为此过程发生的反应是Na2CO3+2HCl=2NaCl+H2O+CO2↑,所以此质量差即是生成二氧化碳的质量;
②设生成4.4g二氧化碳时需要碳酸钠的质量是x
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 44
x 4.4g
| 106 |
| 44 |
| x |
| 4.4g |
x=10.6g
所以食用纯碱粉末中Na2CO3的质量分数为
| 10.6g |
| 11g |
③通过以上计算可知如果测得的结果比实际纯度高,则是测量的二氧化碳质量比实际值偏大,可能的原因是稀盐酸挥发出的HCl气体随CO2气体排出,从而导致所测纯度偏大;
故答案为:(1)红;食用纯碱(或Na2CO3);pH试纸;
(2)乙; 2NaHCO3
| ||
(3)①4.4;②食用纯碱粉末中Na2CO3的质量分数为96.4%;③稀盐酸挥发出的HCl气体随CO2气体排出,从而导致所测纯度偏大.(或水蒸气随CO2气体排出,从而导致所测纯度偏大)
点评:此题是一道实验探究题,解题的关键是利用相关题目中的信息结合探究过程中有关的反应进行分析判断,题目难度不大,注重基础,能较好的训练和强化学生所学的基础知识.

练习册系列答案
相关题目
(2012?盐城)某兴趣小组对食用纯碱和食用小苏打两种粉末进行以下探究.
[查阅资料]
| 名称 | 食用纯碱 | 食用小苏打 |
| 主要成分 | Na2CO3 | NaHCO3 |
| 酸碱性 | 水溶液显碱性 | 水溶液显碱性 |
| 热稳定性 | 受热不分解 | 270℃时完全分解为碳酸钠、二氧化碳、水 |
小明分别向等浓度的两种溶液中滴入酚酞试液,发现两者都变 色,但食用纯碱溶液中颜色更深,由此推测可能 溶液碱性更强.小欢认为要比较两种溶液的碱性强弱,可直接用 进行测定.
(2)验证两种粉末的稳定性
在老师的指导下,该小组按如图1装置进行实验操作,观察到 (填“甲”或“乙”)烧杯中澄清石灰水变浑浊,试管中发生反应的化学方程式为 ,装置中棉花的作用是 .
(3)测定食用纯碱粉末的纯度
取食用纯碱粉末试样,利用如图2装置进行实验测定.
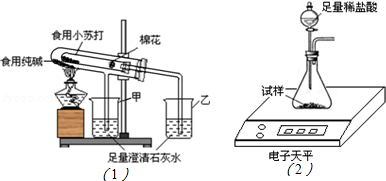
数据记录如下:
| 称量项目 | 称量时间 | 质量/g |
| 试样 | | 11.0 |
| 装置+稀盐酸 | | 160.0 |
| 装置+稀盐酸+试样 | 反应开始后20s | 167.0 |
| 装置+稀盐酸+试样 | 反应开始后30s | 166.6 |
| 装置+稀盐酸+试样 | 反应开始后90s | 166.6 |
③如果测得的结果比实际纯度高,可能的原因是 .(答一种即可)