题目内容
煅烧黄铁矿(主要成分是FeS2)的化学方程式是:4FeS2 + 11O2  2 M + 8 SO2,请判断M的化学式是( )
2 M + 8 SO2,请判断M的化学式是( )
| A.FeSO4 | B.Fe2O3 | C.Fe3O4 | D.Fe2(SO4)3 |
B
解析试题分析:由反应的化学方程式4FeS2 + 11O2  2M + 8SO2可知,
2M + 8SO2可知,
反应前 反应后
Fe原子 4 0
S原子 8 8
O原子 22 16
根据质量守恒定律,化学变化前后原子的种类、数目不变,可判断反应物2M分子中含有4个Fe原子和6个O原子,则1个M分子中含有2个Fe原子和3个O原子,故物质M的化学式为Fe2O3。故选B
考点:质量守恒定律及其应用
点评:本题考查化学式的推断,利用质量守恒定律中的原子守恒来推断是常用的方法,学生应注意守恒思想在解题中的重要作用。

练习册系列答案
相关题目
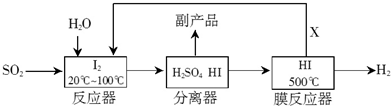
工业上可用煅烧黄铁矿(主要成分FeS2)产生的二氧化硫通过下列工艺过程制取氢气.(碘的化学式:I2)下列说法正确的是( )


| A、分离器中的副产品是H2SO4 | B、膜反应器中发生反应的方程式是2HI?H2+I2 | C、该工艺对于减少二氧化硫排放无影响 | D、生产流程中可以被循环利用的物质是I2 |
 2M+8SO2.请判断M的化学式是( )
2M+8SO2.请判断M的化学式是( )