题目内容
某校化学兴趣小组同学发现,长期使用的热水壶底部有一层水垢,水垢的主要成分是碳酸钙和氢氧化镁.他们为了测定水垢中碳酸钙的含量,将足量的盐酸加入到12.5g水垢中,产生3.3g CO2气体.问水垢中碳酸钙的质量分数是多少?
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:根据反应的化学方程式,由放出二氧化碳的质量计算出样品中碳酸钙质量,碳酸钙质量与水垢样品质量比可计算水垢中碳酸钙的质量分数.
解答:解:设12.5g水垢中碳酸钙的质量为x
CaCO3+2HCl═CaCl2+CO2↑+H2O
100 44
x 3.3g
=
x=7.5g
水垢中碳酸钙的质量分数=
×100%=60%
答:水垢中碳酸钙的质量分数是60%.
CaCO3+2HCl═CaCl2+CO2↑+H2O
100 44
x 3.3g
| 100 |
| x |
| 44 |
| 3.3g |
x=7.5g
水垢中碳酸钙的质量分数=
| 7.5g |
| 12.5g |
答:水垢中碳酸钙的质量分数是60%.
点评:本题主要考查有关化学方程式的计算,难度稍大.

练习册系列答案
相关题目
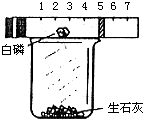 某同学用图所示的装置粗略地测定空气中氧气的体积分数.图中烧杯上方玻璃管(预先固定好)中部有一可左右滑动的活塞,活塞左端管内密封有空气,活塞右端的玻璃管口跟空气连通,实验开始前活塞处在刻度5cm处.(提示:向烧杯内加入适量水,与生石灰反应放出大量的热点燃白磷.)
某同学用图所示的装置粗略地测定空气中氧气的体积分数.图中烧杯上方玻璃管(预先固定好)中部有一可左右滑动的活塞,活塞左端管内密封有空气,活塞右端的玻璃管口跟空气连通,实验开始前活塞处在刻度5cm处.(提示:向烧杯内加入适量水,与生石灰反应放出大量的热点燃白磷.)