题目内容
【题目】为验证氢氧化钠与盐酸反应,化学兴趣小组同学用各自实验台上提供的药品进行了如下实验探究和微观探析。
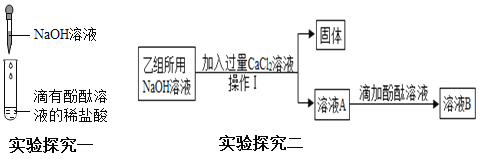
(实验探究一)
(1)甲组同学进行实验一时,向滴有酚酞溶液的稀盐酸中滴加NaOH溶液,振荡后液仍为无色,此现象_____(填“能”或“不能”)证明氢氧化钠与盐酸发生了反应。
(2)乙组同学进行实验一时,还发现试管中出现了“怪现象”——有气泡产生。同学们通过讨论一致认为乙组同学所用的NaOH溶液已变质,其变质的原因是_____。
(提出问题)变质的NaOH溶液中含有哪些溶质?
(作出猜想)猜想一:_____;猜想二:NaOH、Na2CO3
(查阅资料)1.CaCl2溶液显中性。
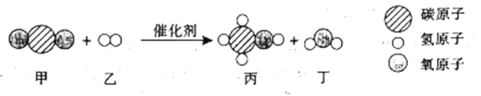
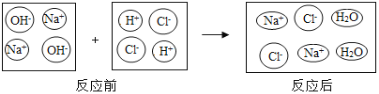
2.稀盐酸和氢氧化钠溶液反应的微观变化如下图所示。
(实验探究二)
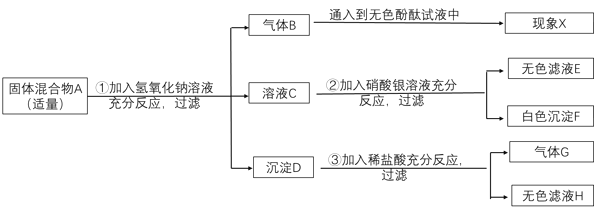
①操作I的名称是_____。
②滴加酚酞溶液后的现象为_____,证明猜想二成立。
③小丹同学用CuSO4溶液代替酚酞溶液也证明了猜想二成立,写出此反应的化学方程式_____。
(反思交流)实验室的化学药品应密封保存。
(微观探析)分析图中反应前后没有发生变化的微粒是钠离子和氯离子,反应的实质是_____(用离子方程式表示)。
【答案】能 氢氧化钠会与空气中的二氧化碳反应 Na2CO3 过滤 溶液B变成红色 CuSO4+2NaOH=Cu(OH)2↓+Na2SO4. H++OH-=H2O
【解析】
【实验探究一】
(1)碱性溶液能使酚酞变红色,所以甲组同学向滴有酚酞溶液的稀盐酸中滴加NaOH溶液,振荡后溶液仍为无色,此现象能证明氢氧化钠与盐酸发生了反应;
(2)氢氧化钠变质是与空气中二氧化碳反应生成碳酸钠和水;
【作出猜想】氢氧化钠可能部分变质,可能全部变质,所以猜想一:Na2CO3;
【实验探究二】①过滤可以将不溶性固体从溶液中分离出来,所以操作I的名称是过滤;
②因为碳酸钠被过量的氯化钙反应完全,无色酚酞变红说明溶液中含有氢氧化钠;所以滴加酚酞溶液后的现象为溶液B变成红色,证明猜想二成立;
③氢氧化钠和硫酸铜反应生成氢氧化铜沉淀和硫酸钠,化学方程式为:CuSO4+2NaOH=Cu(OH)2↓+Na2SO4;
【微观探析】图中反应前后没有发生变化的微粒是钠离子、氯离子,反应的实质是氢离子和氢氧根离子结合生成水分子,离子方程式为H++OH-=H2O。
故答案为:(1)能;
(2)氢氧化钠会与空气中的二氧化碳反应;
【作出猜想】Na2CO3;
【实验探究二】①过滤;
②溶液B变成红色;
③CuSO4+2NaOH=Cu(OH)2↓+Na2SO4。
【微观探析】
H++OH-=H2O。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】镁、铝、锌、铁与稀盐酸或稀硫酸之间的反应规律及图象正确的是( )
|
|
|
|
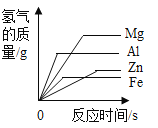
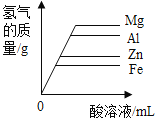
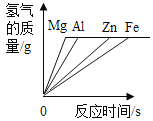
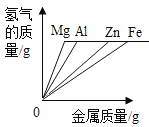
A等质量的镁、铝、锌、铁与足量酸反应,氢气质量与反应时间的关系图象 | B等质量的镁、铝、锌、铁与足量酸反应,氢气质量与酸溶液的关系图象 | C等量酸与足量镁、铝、锌、铁反应,氢气质量与反应时间的关系图象 | D等量酸与足量镁、铝、锌、铁反应,氢气质量与金属质量的关系图象 |
A.AB.BC.CD.D