题目内容
已知金属钠与水在常温下反应的化学方程式为:2Na+2H2O═2NaOH+H2↑.若要得到2g氢气,需要金属钠多少克?
【答案】分析:根据题意,找到已知量是生成的氢气的质量,待求量是参加反应的金属钠的质量,依据题给化学方程式按步骤解答、计算即可.
解答:解:设需要金属钠的质量为x.
2Na+2H2O=2NaOH+H2↑
46 2
x 2g
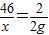
x=46g
答:需要金属钠的质量为46g.
点评:此题主要考查根据化学方程式的计算,注意解题的格式、步骤要规范标准.
解答:解:设需要金属钠的质量为x.
2Na+2H2O=2NaOH+H2↑
46 2
x 2g
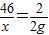
x=46g
答:需要金属钠的质量为46g.
点评:此题主要考查根据化学方程式的计算,注意解题的格式、步骤要规范标准.

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目