题目内容
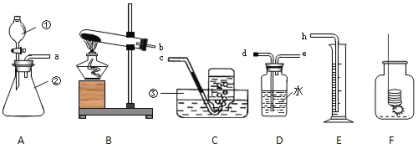
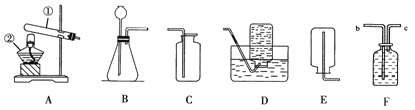
【题目】(9分)实验室常用下列装置制取气体,请根据所学知识回答问题。
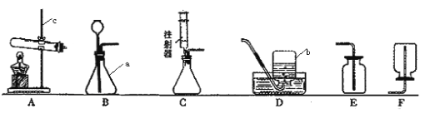
(1)写出有标号仪器的名称:a________________。
(2)A装置的试管口为什么要略向下倾斜? 。
(3)实验室用过氧化氢溶液和二氧化锰粉末混合制取氧气,若选用C而不选B做气体发生装置,其优点是 。
(4)若连接B和F装置,还可以制取另一种气体单质,该气体被认为是未来最理想的清洁能源,反应的方程式为 。
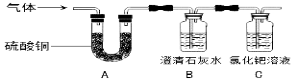
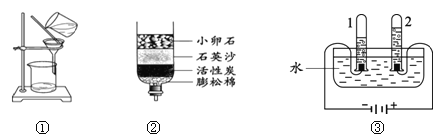
(5)汽车尾气中的一氧化氮是一种大气污染物。它是一种无色气体,难溶于水,密度比空气略大,在空气中能与氧气迅速反应生成红棕色的二氧化氮气体。实验室中制取一氧化氮采用的收集装置是(填序号) 。
(6)若某气体只能用E装置来收集,该气体的性质是 。
(7)在医院里给病人输氧时,在氧气钢瓶和病人吸氧器之间连接一个类似下图所示的装置,在装置中盛放大约半瓶蒸馏水,导气管 (填“长”或“短”)端应连接在供氧气的钢瓶上。若将该装置内装满水,用排水法来收集氧气,则氧气应该从 (填“长”或“短”)端通入。
![]()
【答案】(1)锥形瓶 (2)防止冷凝水倒流使试管炸裂 (3)可以控制反应的发生和停止,节约药品。
(4)Zn+H2SO4===ZnSO4+H2↑ (5)D (6)易溶于水,密度大于空气 (7)长、短
【解析】
试题分析:(2)加热固体时试管口要略向下倾斜,目的是防止冷凝水倒流使试管炸裂;
(3)过氧化氢接触到二氧化锰后,反应便立即开始,不能人为控制其速率和生成氧气的量,故要控制其反应速率,可通过控制过氧化氢的加入量来实现;注射器就可以控制加入液体药品的量和速率;
(4)未来最理想的清洁能源是氢气,实验室一般用锌和稀硫酸反应制取氢气,反应的化学方程式为:Zn+H2SO4===ZnSO4+H2↑;
(5)一氧化氮难溶于水,可用排水法收集;密度比空气略大,在空气中能与氧气迅速反应,不能用向上排空气法收集;
(6)E装置是向上排空气法收集气体的装置,某气体只能用E装置来收集说明该气体易溶于水,密度大于空气;
(7)氧气难溶于水,可通过气泡产生的快慢来判断通入的氧气的速率;将该装置内装满水,用排水法来收集氧气,水只能从长导管排出,故气体从短导管通入。