题目内容
【题目】化学兴趣小组欲探究自己使用的某品牌牙膏的主要成分。
(1)【查阅资料】
①牙膏的成分有活性物质、摩擦剂、保持牙膏湿润的甘油等物质。
②常用的牙膏摩擦剂的主要成分有CaCO3、Al(OH)3、Si02。
③牙膏除了碳酸钙以外,其他物质均不与稀盐酸反应产生气体。
④SiO2不溶于水,也不与盐酸反应。
Al(OH)3和氢氧化钠溶液反应生成偏铝酸钠(NaAlO2)和水,该反应的化学方程式为。
(2)偏铝酸钠和适量稀盐酸反应生成氢氧化铝,氢氧化铝和稀盐酸可以发生中和反应。
相关物质的溶解性表:
物质 | Al(OH)3 | NaAlO2 | AlCl3 |
溶解性 | 不溶 | 溶 | 溶 |
该品牌牙膏含有上述摩擦剂中的两种成分,为探究摩擦剂的组成,化学兴趣小组取适量该牙膏加水充分搅拌、静置、过滤、洗涤、干燥,得到该牙膏中的摩擦剂.
【提出猜想】猜想1:摩擦剂的成分为Al(OH)3和CaCO3 .
猜想2:摩擦剂的成分为 .
猜想3:摩擦剂的成分为SiO2和Al(OH)3 .
【设计实验】
实验步骤 | 预期实验现象 | 预期实验结论 |
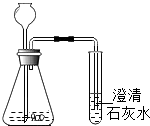
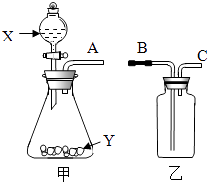
组装下图装置进行实验.取少量摩擦剂于锥形瓶中,加入适量的 . | 固体全部溶解,有气泡,石灰水变浑浊 | 则猜想1成立 |
摩擦剂部分溶解 | 则猜想3成立 |
【实验结论】经过实验验证,猜想1成立.
【实验反思】同学们为进一步确认摩擦剂中含有氢氧化铝,先在少量牙膏样品中加入过量的氢氧化钠溶液,静置一段时间,取上层清液,再滴加稀盐酸至过量.整个实验过程中观察到的现象为 , 依据该现象可以判断摩擦剂中一定含有氢氧化铝.
【答案】
(1)Al(OH)3+NaOH=NaAlO2+2H2O
(2)SiO2和CaCO3,稀盐酸,Al(OH)3+3HCl=AlCl3+3H2O,CaCO3+2HCl=CaCl2+H2O+CO2↑,牙膏样品中部分固体溶解,向上层清液中滴加稀盐酸时开始无现象,之后有固体产生,最后固体溶解
【解析】SiO2不溶于水,也不与盐酸反应。Al(OH)3和氢氧化钠溶液反应生成偏铝酸钠(NaAlO2)和水,该反应的化学方程式为Al(OH)3+NaOH=NaAlO2+2H2O;常用的牙膏摩擦剂的主要成分有CaCO3、Al(OH)3、SiO2。可能的情况是三种:猜想1:摩擦剂的成分为Al(OH)3和CaCO3。猜想2:摩擦剂的成分为SiO2和CaCO3。猜想3:摩擦剂的成分为SiO2和Al(OH)3。组装下图装置进行实验。取少量摩擦剂于锥形瓶中,加入适的盐酸,猜想1成立锥形瓶中发生的反应为:Al(OH)3+3HCl=AlCl3+3H2O;CaCO3+2HCl=CaCl2+H2O+CO2↑;为进一步确认摩擦剂中含有氢氧化铝,先在少量牙膏样品中加入过量的氢氧化钠溶液,静置一段时间,取上层清液,再滴加稀盐酸至过量。整个实验过程中观察到的现象为牙膏样品中部分固体溶解,向上层清液中滴加稀盐酸时开始无现象,之后有固体产生,最后固体溶解,依据该现象可以判断摩擦剂中一定含有氢氧化铝.
故答案为:Al(OH)3+NaOH=NaAlO2+2H2O;SiO2和CaCO3;稀盐酸;Al(OH)3+3HCl=AlCl3+3H2O;CaCO3+2HCl=CaCl2+H2O+CO2↑;牙膏样品中部分固体溶解,向上层清液中滴加稀盐酸时开始无现象,之后有固体产生,最后固体溶解.
牙膏摩擦剂的主要成分有CaCO3、Al(OH)3、SiO2,根据由上边物质中的两种组成,进行两种物质的组合考虑;根据预期实验结论猜想1正确,用猜想1的成分与盐酸反应考虑实验现象;根据若摩擦剂部分溶解,不产生气泡,说明不存在碳酸钙考虑哪一猜想正确;(1)根据方程式的写法考虑;(2)根据硫酸与碳酸钙反应的生成物考虑.