题目内容
(2011?玄武区二模)2014年青奥会将在南京举行,为了控制汽车尾气给空气造成的污染,南京市在燃料的使用和管理等方面采取了一些有效措施.
(1)图1中公交车使用的天然气主要成分是______,其完全燃烧的化学方程式为______ CO2+2H2O
【答案】分析:(1)天然气的主要成分是甲烷,甲烷燃烧能生成水和二氧化碳.
(2)氢气燃烧能生成水,目前生产氢气的方法价格较高,氢气不容易贮存.
(3)根据表中数据可以进行相关方面的计算、判断;根据物质的化学式可以计算某种元素的质量分数.
解答:解:(1)图1中公交车使用的天然气主要成分是甲烷;甲烷完全燃烧的化学方程式为:CH4+2O2 CO2+2H2O.
CO2+2H2O.
故答案为:甲烷;CH4+2O2 CO2+2H2O;
CO2+2H2O;
(2)氢气在空气中燃烧的化学方程式为:2H2+O2 2H2O.
2H2O.
氢动力汽车目前还不能普及,原因是没有找到比较经济的生产氢气的方法,氢气不易贮存等.
故答案为:2H2+O2 2H2O;成本高(贮存困难;不纯易爆等,其他合理的答案也给分)
2H2O;成本高(贮存困难;不纯易爆等,其他合理的答案也给分)
(3)由表中数据和质量守恒定律可知,乙醇和氧气反应能生成一氧化碳、二氧化碳和水,反应的化学方程式为:2C2H5OH+5O2 2CO2+2CO+6H2O.
2CO2+2CO+6H2O.
解:设生成二氧化碳、一氧化碳水的质量分别为X、Y、Z.
2C2H5OH+5O2 2CO2+2CO+6H2O.
2CO2+2CO+6H2O.
160 88 56 108
40g X Y Z
 =
= =
= =
=
X=22g,Y=14g,Z=27g.
由此可知,Y是一氧化碳,其中碳元素和氧元素的质量比为:12:16=3:4.
乙醇中碳元素的质量分数为: ×100%=52.2%;
×100%=52.2%;
汽油中碳元素的质量分数为: ×100%=84.2%.
×100%=84.2%.
则相同条件下,乙醇和汽油分别燃烧时,产生CO较多的是汽油.
足够多的氧气或增大可燃物与氧气的接触面积可以促进可燃物燃烧.
故答案为:3:4;汽油;足够多的氧气(或与氧气有足够大的接触面积)(其他合理的答案也给分).
点评:本题主要考查化学方程式的书写方法和相关方面的计算,书写化学方程式时要遵循质量守恒定律.
(2)氢气燃烧能生成水,目前生产氢气的方法价格较高,氢气不容易贮存.
(3)根据表中数据可以进行相关方面的计算、判断;根据物质的化学式可以计算某种元素的质量分数.
解答:解:(1)图1中公交车使用的天然气主要成分是甲烷;甲烷完全燃烧的化学方程式为:CH4+2O2
 CO2+2H2O.
CO2+2H2O.故答案为:甲烷;CH4+2O2
 CO2+2H2O;
CO2+2H2O;(2)氢气在空气中燃烧的化学方程式为:2H2+O2
 2H2O.
2H2O. 氢动力汽车目前还不能普及,原因是没有找到比较经济的生产氢气的方法,氢气不易贮存等.
故答案为:2H2+O2
 2H2O;成本高(贮存困难;不纯易爆等,其他合理的答案也给分)
2H2O;成本高(贮存困难;不纯易爆等,其他合理的答案也给分)(3)由表中数据和质量守恒定律可知,乙醇和氧气反应能生成一氧化碳、二氧化碳和水,反应的化学方程式为:2C2H5OH+5O2
 2CO2+2CO+6H2O.
2CO2+2CO+6H2O.解:设生成二氧化碳、一氧化碳水的质量分别为X、Y、Z.
2C2H5OH+5O2
 2CO2+2CO+6H2O.
2CO2+2CO+6H2O.160 88 56 108
40g X Y Z
 =
= =
= =
=
X=22g,Y=14g,Z=27g.
由此可知,Y是一氧化碳,其中碳元素和氧元素的质量比为:12:16=3:4.
乙醇中碳元素的质量分数为:
 ×100%=52.2%;
×100%=52.2%;汽油中碳元素的质量分数为:
 ×100%=84.2%.
×100%=84.2%.则相同条件下,乙醇和汽油分别燃烧时,产生CO较多的是汽油.
足够多的氧气或增大可燃物与氧气的接触面积可以促进可燃物燃烧.
故答案为:3:4;汽油;足够多的氧气(或与氧气有足够大的接触面积)(其他合理的答案也给分).
点评:本题主要考查化学方程式的书写方法和相关方面的计算,书写化学方程式时要遵循质量守恒定律.

练习册系列答案
相关题目
(2011?玄武区二模)知识在于积累,下面是聪聪同学制作的化学知识卡片,请将其补充完整.
| 专题2:物质的性质和用途 No:WZ09 摘录时间2011年3月20日 (1)工业用盐 致癌作用 含______价氮 该物质的化学式NaNO2 (2)制取氧气 暗紫色固体 可用于消毒的盐 该物质的化学式______ (3)无色无味 剧毒气体 与血红蛋白结合 该物质的化学式______ (4)一种氮肥 含氮______% 溶于水温度下降 该物质的化学式NH4NO3 |
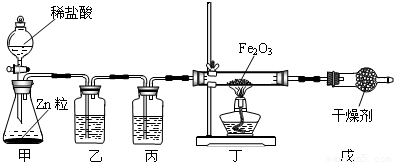


 (2011?玄武区二模)金属材料在生产、生活中有着广泛的应用.
(2011?玄武区二模)金属材料在生产、生活中有着广泛的应用.