题目内容
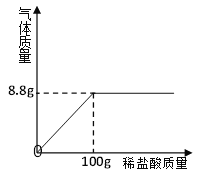
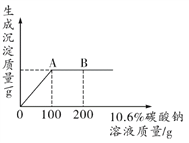
【题目】向50g 由氯化钠和氯化钡组成的固体混合物中逐滴滴加10.6%的碳酸钠溶液,所加碳酸钠溶液质量与生成沉淀质量的关系见下图。
提示:( BaCl2 + Na2CO3 = BaCO3↓ + 2NaCl )
(1)图中表示恰好完全反应的点是______。(填“A”或“B”)
(2)求生成沉淀的质量________。
(3)求恰好完全反应时所得溶液中溶质的质量分数_______。(精确到0.1%)
【答案】 A 19.7 31.4%
【解析】(1)由图像可知,A点后沉淀质量不再增多,故A点表示恰好反应。
(2)设生成沉淀的质量为x。
BaCl2 + Na2CO3 = BaCO3↓ + 2NaCl
106 197
100g×10.6% x
![]() =
=![]() ,解得x=19.7g
,解得x=19.7g
(3)设反应生成氯化钠的质量为y,混合物中氯化钡的质量为w。
BaCl2 + Na2CO3 = BaCO3↓ + 2NaCl
208 106 117
w 100g×10.6% y
![]() =
= ![]() ,解得w=20.8g
,解得w=20.8g
![]() =
=![]() ,解得y=11.7g
,解得y=11.7g
混合物中氯化钠的质量为:50g-20.8g=29.2g
恰好完全反应时所得溶液中溶质的质量:29.2g+11.7g=40.9g
恰好完全反应时所得溶液的质量:50g+100g-19.7g=130.3g
恰好完全反应时所得溶液中溶质的质量分数:![]() ×100%=31.4%
×100%=31.4%

练习册系列答案
 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案
相关题目