题目内容
在实验室里,某同学看到氢氧化钠试剂瓶的瓶口有白色粉末,他对白色粉末的成分作出猜测.猜测一:可能是氧氧化钠;猜测二:可能是碳酸钠 猜测三:可能是氧氧化钠和碳酸钠.为探究白色粉末的成分,他将该粉末溶于水,得到无色溶液,再迸行了如下实验: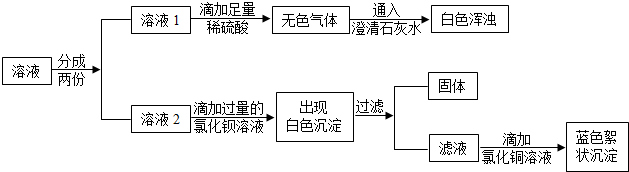
(1)根据实验现象推测,无色气体是 .
(2)在溶液2中滴加过量氯化钡溶液的目的是
(3)由实验现象可知,猜测 是正确的.
(4)假设猜想二是正确的,请设计实验验证 (只需要写出实验步骤)

(1)根据实验现象推测,无色气体是
(2)在溶液2中滴加过量氯化钡溶液的目的是
(3)由实验现象可知,猜测
(4)假设猜想二是正确的,请设计实验验证
考点:实验探究物质的组成成分以及含量,碱的化学性质,盐的化学性质
专题:科学探究
分析:(1)碳酸钠和稀硫酸反应生成硫酸钠、水和二氧化碳;
(2)滴加过量的氯化钡溶液时,碳酸钠能够完全反应,从而防止了对氢氧化钠检验的干扰;
(3)根据实验现象可以判断白色粉末的组成;
(4)如果白色粉末是碳酸钠,和过量的氯化钙反应后,溶液显中性,不能使酚酞试液变色.
(2)滴加过量的氯化钡溶液时,碳酸钠能够完全反应,从而防止了对氢氧化钠检验的干扰;
(3)根据实验现象可以判断白色粉末的组成;
(4)如果白色粉末是碳酸钠,和过量的氯化钙反应后,溶液显中性,不能使酚酞试液变色.
解答:解:(1)根据实验现象推测,无色气体是碳酸钠和稀硫酸反应生成的二氧化碳,因为即使白色粉末中含有氢氧化钠,氢氧化钠和稀硫酸反应也不能生成气体.
故填:二氧化碳.
(2)在溶液2中滴加过量氯化钡溶液的目的是使碳酸钠完全反应.
故填:使碳酸钠完全反应.
(3)由实验现象可知,白色粉末中含有碳酸钠和氢氧化钠,猜测三是正确的.
故填:三.
(4)假设猜想二是正确的,设计实验验证方法是:
实验步骤:滴加过量的氯化钙溶液,再滴加几滴酚酞试液;
实验现象:产生白色沉淀,酚酞试液不变色;
实验结论:白色粉末是碳酸钠.
故填:滴加过量的氯化钙溶液,再滴加几滴酚酞试液.
故填:二氧化碳.
(2)在溶液2中滴加过量氯化钡溶液的目的是使碳酸钠完全反应.
故填:使碳酸钠完全反应.
(3)由实验现象可知,白色粉末中含有碳酸钠和氢氧化钠,猜测三是正确的.
故填:三.
(4)假设猜想二是正确的,设计实验验证方法是:
实验步骤:滴加过量的氯化钙溶液,再滴加几滴酚酞试液;
实验现象:产生白色沉淀,酚酞试液不变色;
实验结论:白色粉末是碳酸钠.
故填:滴加过量的氯化钙溶液,再滴加几滴酚酞试液.
点评:实验现象是物质之间相互作用的外在表现,因此要学会设计实验、观察实验、分析实验,为揭示物质之间相互作用的实质奠定基础.

练习册系列答案
相关题目
下列物质的性质属于化学性质的是( )
| A、氧气密度比空气密度略大 |
| B、氢气难溶于水 |
| C、白磷能在空气中自燃 |
| D、氧气是无色无味气体 |
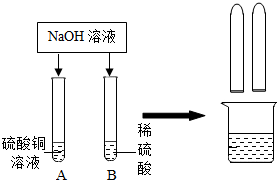 某化学小组在探究碱的化学性质时,做了如图所示的两个实验.
某化学小组在探究碱的化学性质时,做了如图所示的两个实验.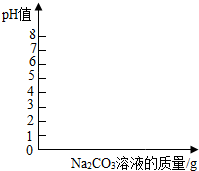 某兴趣小组需要配制100g质量分数为9.8%的稀硫酸,假设常温下该稀硫酸的pH值为0.在装有100g该稀硫酸的烧杯中加入104.4gNa2CO3溶液,恰好完全反应,溶液呈中性.
某兴趣小组需要配制100g质量分数为9.8%的稀硫酸,假设常温下该稀硫酸的pH值为0.在装有100g该稀硫酸的烧杯中加入104.4gNa2CO3溶液,恰好完全反应,溶液呈中性.