题目内容
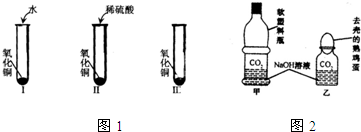
22、化学复习课上,老师将CO2分别通入澄清的石灰水和NaOH溶液中,我们观察到前者变浑浊,后者无明显现象,CO2和NaOH是否确实发生了化学反应?

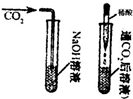
(1)我设计了甲、乙两个实验来验证,如如图所示,实验现象为:甲-软塑料瓶变瘪,乙-“瓶吞鸡蛋”.
小虎同学认为上述实验是可行的,其共同原理是:
(2)小余同学认为可利用与上述实验不同的原理,设计如下实验方案,我来帮他完成:
写出方案2中所涉及的化学方程式

(1)我设计了甲、乙两个实验来验证,如如图所示,实验现象为:甲-软塑料瓶变瘪,乙-“瓶吞鸡蛋”.
小虎同学认为上述实验是可行的,其共同原理是:
都是一个密闭的体系里设法消耗CO2,使得气体压强减少,从而观察到明显现象;
小余同学提出了质疑,他认为上述实验还不足以证明CO2与NaOH确实发生了反应,其理由是:CO2能溶于水,究竟是CO2溶于水使气压减小的结果?还是CO2与NaOH反应使气压减小的结果?
我思考后,又补充了一个实验来回答,这个实验是:做个对比实验:取一个与甲装置同样大小的软塑料瓶,充满CO2后,注入与氢氧化钠溶液体积相同的水,振荡,比较瓶子变瘪的程度,即可判断.
.(2)小余同学认为可利用与上述实验不同的原理,设计如下实验方案,我来帮他完成:
| 实验步骤和方法 | 实验现象 | 实验结论 | |
| 方案1 |  |
① 产生气泡 |
C02和NaOH 确实发生了 化学反应 |
| 方案2 | ② 将CO2通入NaOH溶液后,再滴加CaCl2溶液 |
③ 产生白色沉淀 |
CO2+2NaOH=Na2CO3+H2O,Na2CO3+CaCl2=CaCO3↓+2NaCl
.分析:(1)二氧化碳能和氢氧化钠溶液反应生成碳酸钠和水,通过容器中压强的变化可以进行判断;
(2)二氧化碳能和氢氧化钠溶液反应生成碳酸钠和水,碳酸钠能和氯化钙反应生成碳酸钙和氯化钠.
(2)二氧化碳能和氢氧化钠溶液反应生成碳酸钠和水,碳酸钠能和氯化钙反应生成碳酸钙和氯化钠.
解答:解:(1)小虎同学认为上述实验是可行的,其共同原理是:都是一个密闭的体系里设法消耗CO2,使得气体压强减少,从而观察到明显现象;故填:都是一个密闭的体系里设法消耗CO2,使得气体压强减少,从而观察到明显现象;
小余同学提出了质疑,他认为上述实验还不足以证明CO2与NaOH确实发生了反应,其理由是:CO2能溶于水,究竟是CO2溶于水使气压减小的结果?还是CO2与NaOH反应使气压减小的结果?故填:CO2能溶于水,究竟是CO2溶于水使气压减小的结果?还是CO2与NaOH反应使气压减小的结果?
我思考后,又补充了一个实验来回答,这个实验是:做个对比实验:取一个与甲装置同样大小的软塑料瓶,充满CO2后,注入与氢氧化钠溶液体积相同的水,振荡,比较瓶子变瘪的程度,即可判断. 故填:做个对比实验:取一个与甲装置同样大小的软塑料瓶,充满CO2后,注入与氢氧化钠溶液体积相同的水,振荡,比较瓶子变瘪的程度,即可判断.
(2)①碳酸钠和稀酸反应能生成二氧化碳气体.故填:产生气泡.
②将CO2通入NaOH溶液后,再滴加CaCl2溶液可以检验二氧化碳是否与氢氧化钠发生了反应.故填:将CO2通入NaOH溶液后,再滴加CaCl2溶液.
③碳酸钠能和氯化钙反应生成沉淀碳酸钙和氯化钠.故填:产生白色沉淀.
方案2中所涉及的化学方程式为:CO2+2NaOH=Na2CO3+H2O,Na2CO3+CaCl2=CaCO3↓+2NaCl.
小余同学提出了质疑,他认为上述实验还不足以证明CO2与NaOH确实发生了反应,其理由是:CO2能溶于水,究竟是CO2溶于水使气压减小的结果?还是CO2与NaOH反应使气压减小的结果?故填:CO2能溶于水,究竟是CO2溶于水使气压减小的结果?还是CO2与NaOH反应使气压减小的结果?
我思考后,又补充了一个实验来回答,这个实验是:做个对比实验:取一个与甲装置同样大小的软塑料瓶,充满CO2后,注入与氢氧化钠溶液体积相同的水,振荡,比较瓶子变瘪的程度,即可判断. 故填:做个对比实验:取一个与甲装置同样大小的软塑料瓶,充满CO2后,注入与氢氧化钠溶液体积相同的水,振荡,比较瓶子变瘪的程度,即可判断.
(2)①碳酸钠和稀酸反应能生成二氧化碳气体.故填:产生气泡.
②将CO2通入NaOH溶液后,再滴加CaCl2溶液可以检验二氧化碳是否与氢氧化钠发生了反应.故填:将CO2通入NaOH溶液后,再滴加CaCl2溶液.
③碳酸钠能和氯化钙反应生成沉淀碳酸钙和氯化钠.故填:产生白色沉淀.
方案2中所涉及的化学方程式为:CO2+2NaOH=Na2CO3+H2O,Na2CO3+CaCl2=CaCO3↓+2NaCl.
点评:本题主要探究二氧化碳能否与氢氧化钠反应及其化学方程式的书写等方面的知识,书写化学方程式时要注意遵循质量守恒定律.

练习册系列答案
相关题目

 30、化学复习课上,老师将CO2分别通入澄清的石灰水和NaOH溶液中,我们观察到前者变浑浊,后者无明显现象.CO2和NaOH是否确实发生了化学反应?
30、化学复习课上,老师将CO2分别通入澄清的石灰水和NaOH溶液中,我们观察到前者变浑浊,后者无明显现象.CO2和NaOH是否确实发生了化学反应?
 (2008?怀柔区一模)化学复习课上,老师将CO2分别通入澄清的石灰水和NaOH溶液中,观察到前者变浑浊,后者无明显现象,同学们展开了探究.
(2008?怀柔区一模)化学复习课上,老师将CO2分别通入澄清的石灰水和NaOH溶液中,观察到前者变浑浊,后者无明显现象,同学们展开了探究.