题目内容
【题目】为减少污染并变废为宝,某化学小组在实验室探究工业废水的综合利用,设计了以下流程图并完成了回收铜和硫酸锌的实验.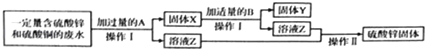
(1)X的成分为;操作Ⅰ需用的玻璃仪器有烧杯、玻璃棒和 .
(2)加入B时反应的化学方程式为 .
(3)操作Ⅱ中玻璃棒的作用是 .
【答案】
(1)锌、铜;漏斗
(2)Zn+H2SO4=ZnSO4+H2↑
(3)搅拌,防止局部过热,造成液滴飞溅
【解析】(1)锌和硫酸铜反应生成硫酸锌和铜,所以加入的A是锌,所以X的成分为锌、铜,操作Ⅰ分离出了固体和溶液,所以操作I是过滤,需用的玻璃仪器有烧杯、玻璃棒和漏斗;(2)加入过量的锌可以跟硫酸铜完全反应,但是过量的锌对于铜仍是杂质,锌和稀硫酸反应生成硫酸锌和氢气,化学方程式为:Zn+H2SO4=ZnSO4+H2↑;(3)从溶液中得到固体的方法是蒸发,所以操作Ⅱ中玻璃棒的作用是搅拌,防止局部过热,造成液滴飞溅.
所以答案是:(1)锌、铜,漏斗;(2)Zn+H2SO4=ZnSO4+H2↑;(3)搅拌,防止局部过热,造成液滴飞溅.
【考点精析】关于本题考查的过滤操作的注意事项和蒸发操作的注意事项,需要了解过滤操作注意事项:“一贴”“二低”“三靠;过滤后,滤液仍然浑浊的可能原因有:①承接滤液的烧杯不干净②倾倒液体时液面高于滤纸边缘③滤纸破损;蒸发注意点:1、在加热过程中,用玻璃棒不断搅拌2、当液体接近蒸干(或出现较多量固体)时停止加热,利用余热将剩余水分蒸发掉,以避免固体因受热而迸溅出来.3、热的蒸发皿要用坩埚钳夹取,热的蒸发皿如需立即放在实验台上,要垫上石棉网才能得出正确答案.

 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案【题目】化学兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验(如图),同学们观察到镁条在空气中剧烈燃烧,发出耀眼的强光,产生的大量白烟弥漫到空气中,最后在石棉网上得到一些白色固体. 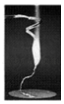
(1)请写出镁条燃烧的化学方程式;
(2)同学们通过称量发现:在石棉网上收集到产物的质量小于镁条的质量,有人认为这个反应不遵循质量守恒定律.你认为出现这样实验结果的原因可能是:
(3)小红按右下图装置改进实验,验证了质量守恒定律,还发现产物中有少量黄色固体. 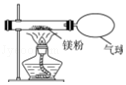
【提出问题】黄色固体是什么?
【查阅资料】①氧化镁为白色固体;②镁能与氮气剧烈反应产生黄色的氮化镁(Mg3N2)固体;③氮化镁可与水反应产生氨气,该气体能使湿润的红色石蕊试纸变蓝.
【做出猜想】黄色固体是Mg3N2
【实验探究】请设计实验,验证猜想
实验操作 | 实验现象及结论 |
(4)【反思与交流】①氮化镁中氮元素的化合价是; ②空气中N2的含量远大于O2的含量,可是镁条在空气中燃烧产物MgO却远多于Mg3N2 , 合理的解释是: .
③同学们又联想到氯气在氧气中能够燃烧,于是对燃烧条件又有了新的认识: .