题目内容
在宏观、微观和符号之间建立联系是化学学科的特点.
(1)从深海鱼油中提取出来的一种不饱和脂肪酸被称为“脑黄金”,它的化学式为C26H40O2,它由
(2)自来水消毒过程中通常会发生如下反应,其反应的微观过程可用图表示:
请回答以下问题:
①以上物质中属于氧化物的是
②乙图所示化学反应中,若生成64gE物质,需要D物质的质量为
(3)在探究铁、铜、锌、银的金属活动性顺序时,某小组做了如图1三个实验:(所用金属的形状与大小和稀盐酸的用量均相同)
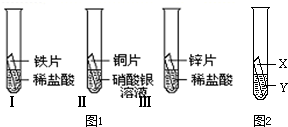
①一段时间后,可观察到实验Ⅱ的现象是
②小组中的甲同学认为:通过实验Ⅰ和Ⅲ可比较出锌和铁的金属活动性强弱.你认为他依据的实验现象是
③乙和丙两位同学认为上述三个实验不能够得出四种金属的活动性顺序,原因是
(1)从深海鱼油中提取出来的一种不饱和脂肪酸被称为“脑黄金”,它的化学式为C26H40O2,它由
三
三
种元素组成,其中氢元素与氧元素的质量比为5:4
5:4
.(2)自来水消毒过程中通常会发生如下反应,其反应的微观过程可用图表示:

请回答以下问题:
①以上物质中属于氧化物的是
A
A
(填序号).②乙图所示化学反应中,若生成64gE物质,需要D物质的质量为
210
210
g.(3)在探究铁、铜、锌、银的金属活动性顺序时,某小组做了如图1三个实验:(所用金属的形状与大小和稀盐酸的用量均相同)

①一段时间后,可观察到实验Ⅱ的现象是
溶液的蓝色消失,铜片上附着银白色金属
溶液的蓝色消失,铜片上附着银白色金属
;反应的化学方程式是Cu+2AgNO3=Cu(NO3)2+2Ag
Cu+2AgNO3=Cu(NO3)2+2Ag
②小组中的甲同学认为:通过实验Ⅰ和Ⅲ可比较出锌和铁的金属活动性强弱.你认为他依据的实验现象是
实验Ⅲ中产生的气体的速率比实验Ⅰ快;
实验Ⅲ中产生的气体的速率比实验Ⅰ快;
.③乙和丙两位同学认为上述三个实验不能够得出四种金属的活动性顺序,原因是
无法比较铁和铜的活动性大小
无法比较铁和铜的活动性大小
;并在上述实验的基础上,补充了一个实验(如图2所示),实现了探究目的.他们的实验:X是金属Fe
Fe
,Y是CuSO4
CuSO4
溶液(写出化学式).分析:(1)依据化学式的意义和有关计算分析解答;
(2)依据反应过程中分子的有关结构书写反应的化学方程式,进而完成相关的计算即可;
(3)①根据金属活动性书序表的应用分析反应,根据反应写出方程式;
②根据金属与酸反应的速度快慢考虑;
③根据每一种实验能得出的结论及比较金属的活动性大小常用的方法分析.
(2)依据反应过程中分子的有关结构书写反应的化学方程式,进而完成相关的计算即可;
(3)①根据金属活动性书序表的应用分析反应,根据反应写出方程式;
②根据金属与酸反应的速度快慢考虑;
③根据每一种实验能得出的结论及比较金属的活动性大小常用的方法分析.
解答:解:(1)依据该物质的化学式为C26H40O2,可知该物质是由碳、氢、氧3种元素组成的;该物质中氢、氧元素的质量比是1×40:16×2=5:4;
(2)根据反应的微观过程反应方程式为:H2O+Cl2=HCl+HClO;2HClO
2HCl+O2↑;
氧化物是指由两种元素组成且其中一种是氧元素的化合物,因此可知,①反应物质中属于氧化物的是A;
设 若生成64gE物质,需要D物质的质量为 x g
2HClO
2HCl+O2↑
105 32
x 64g
=
解答 x=210 g;
(3)①铜与硝酸银反应生成了银和硝酸铜,反应的方程式是:Cu+2AgNO3=Cu(NO3)2+2Ag,故一段时间后的实验现象是溶液的蓝色消失,铜片上附着银白色金属;
②金属与酸反应的速度越快说明该金属越活泼,所以依据的实验现象是:实验Ⅲ中产生的气体的速率比实验Ⅰ快;
③第Ⅰ个实验说明铁排在了氢的前面,第Ⅱ各实验说明铜排在银的前面,第Ⅲ个实验说明锌排在了氢的前面,所以无法比较铁和铜的关系,所以把铁放入铜的盐溶液(硫酸铜等)中看是否反应即可,如果反应,铁就比铜活泼,否则铜比铁活泼.
故答案为:(1)三;5:4;(2)A;210;(3)①溶液的蓝色消失,铜片上附着银白色金属;Cu+2AgNO3=Cu(NO3)2+2Ag;②实验Ⅲ中产生的气体的速率比实验Ⅰ快;③无法比较铁和铜的活动性大小;Fe;CuSO4.
(2)根据反应的微观过程反应方程式为:H2O+Cl2=HCl+HClO;2HClO
| ||
氧化物是指由两种元素组成且其中一种是氧元素的化合物,因此可知,①反应物质中属于氧化物的是A;
设 若生成64gE物质,需要D物质的质量为 x g
2HClO
| ||
105 32
x 64g
| 105 |
| x |
| 32 |
| 64g |
解答 x=210 g;
(3)①铜与硝酸银反应生成了银和硝酸铜,反应的方程式是:Cu+2AgNO3=Cu(NO3)2+2Ag,故一段时间后的实验现象是溶液的蓝色消失,铜片上附着银白色金属;
②金属与酸反应的速度越快说明该金属越活泼,所以依据的实验现象是:实验Ⅲ中产生的气体的速率比实验Ⅰ快;
③第Ⅰ个实验说明铁排在了氢的前面,第Ⅱ各实验说明铜排在银的前面,第Ⅲ个实验说明锌排在了氢的前面,所以无法比较铁和铜的关系,所以把铁放入铜的盐溶液(硫酸铜等)中看是否反应即可,如果反应,铁就比铜活泼,否则铜比铁活泼.
故答案为:(1)三;5:4;(2)A;210;(3)①溶液的蓝色消失,铜片上附着银白色金属;Cu+2AgNO3=Cu(NO3)2+2Ag;②实验Ⅲ中产生的气体的速率比实验Ⅰ快;③无法比较铁和铜的活动性大小;Fe;CuSO4.
点评:此题是一道多点知识考查题,解题的关键是能够利用微观知识以及实验探究的相关要求分析解答;

练习册系列答案
相关题目
在宏观、微观和符号之间建立联系是化学学科的特点.现有A、B、C、D四种物质,其微观示意图见下表.
(1)1个B物质分子中有 原子.
(2)上述物质中属于单质的是 ,属于有机物的是 .[填写化学式]
(3)C物质中两种元素的质量比为 .
(4)将一定质量的A、B、C、D四种物质放在一密闭的容器内中,在电火花作用下,发生充分反应,测得反应前后各物质的质量如下:
其中,a值为 ,该反应的化学方程式中A与D的化学计量数之比为 .
| 物质 | A | B | C | D |  --氢原子 --氢原子 --碳原子 --碳原子 --氧原子 --氧原子 |
| 微观示意图 |  |
 |
 |
 |
(2)上述物质中属于单质的是
(3)C物质中两种元素的质量比为
(4)将一定质量的A、B、C、D四种物质放在一密闭的容器内中,在电火花作用下,发生充分反应,测得反应前后各物质的质量如下:
| A | B | C | D | |
| 反应前质量/g | 25 | 1 | 10 | 74 |
| 反应后质量/g | 9 | 37 | a | 10 |

 ”、“
”、“ ”、“
”、“ ”分别表示A、B、C三种物质的分子,下图表示某化学反应前后反应物与生成物分子及其数目的变化.该化学方程式中A、B、C前的化学计量数之比为
”分别表示A、B、C三种物质的分子,下图表示某化学反应前后反应物与生成物分子及其数目的变化.该化学方程式中A、B、C前的化学计量数之比为

 表示A元素的原子,
表示A元素的原子, 表示B元素的原子.某反应前后的物质微观示意图如下.
表示B元素的原子.某反应前后的物质微观示意图如下.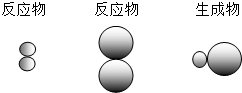
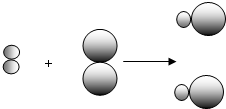 和
和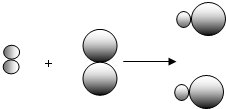 中的
中的 属于同种元素,这是因为这些原子含有相同的
属于同种元素,这是因为这些原子含有相同的 表示甲元素的原子,
表示甲元素的原子, 表示乙元素的原子.某反应前后的物质微观示意图如下.
表示乙元素的原子.某反应前后的物质微观示意图如下.


 属于同种元素,这是因为这些原子含有相同的
属于同种元素,这是因为这些原子含有相同的




