题目内容
【题目】在今年化学实验操作考试“探究纯碱的性质”中,同学们做了如图所示的四组实 验,并将 A、B、C、D 四支试管中的废液全部倒入一个干净的大烧杯中。考试结束后,某兴趣小组发现大烧杯底部有沉淀,上层溶液呈红色。为了探究上层溶液的成分,进行了以下实验。
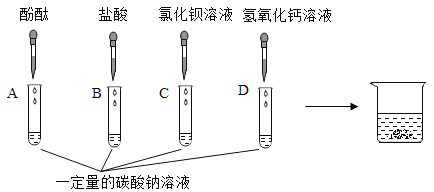
(提出问题)大烧杯中的上层溶液中除了含有水和酚酞外,还含有哪些离子?(假设难溶物质、水和酚酞均不会解离出离子)
(猜想假设)小明认为上层溶液中一定含有 Na+、CO32-、H+、Cl-、Ba2+、Ca2+、OH-七种离子,你认为上层溶液中含有的离子最多可能有______________种。
(分析讨论)小红认为上层溶液中一定不含有H+,因为是____________。小李取一 定量的上层溶液于试管中,滴加几滴稀盐酸,发现无气泡产生,认为上层溶液中一 定不含有CO32-,小红认为他的结论不正确,原因是_______________________。
(设计实验)为进一步确定上层溶液中是否含有CO32-,请你和小红一起参与下列探究
实验操作 | 实验现象 | 实验结论 |
取大烧杯中的上层 溶液少许于一支试 管中,滴加__________, 静置 | ____________;试管中的上层溶液仍是红色 | 大烧杯中的上层溶液中一定含有CO32,发生的化学反应方程式为________ ;同时还能得出大烧杯中的上层溶液中一定含有的阴离子是____ (填 离子符号) |
(实验结论)大烧杯中的上层溶液中一定含有的离子是_____________ (填离子符号)。
【答案】5 上层溶液呈红色或烧杯中有沉淀 上层溶液中含 OH-时,滴加稀盐酸如果不足量也不会有气泡产生 足量(或过量)的BaCl2溶液(合理即可) 产生白色沉淀 ![]() OH- Na+、Cl-、CO32-、OH-
OH- Na+、Cl-、CO32-、OH-
【解析】
盐酸和碳酸钠反应生成氯化钠、水和二氧化碳,碳酸钠和氯化钡反应生成碳酸钡和氯化钠,氢氧化钙和碳酸钠反应生成碳酸钙和氢氧化钠,盐酸和氢氧化钠反应生成氯化钠和水。
[猜想假设]①上层溶液中含有的离子可能组成情况:碳酸钠和盐酸、氯化钡、氢氧化钙恰好完全反应:Na+、Cl、OH;碳酸钠过量:Na+、CO32、Cl、OH;氯化钡过量:Na+、Cl、Ba2+、OH;氢氧化钙过量:Na+、Cl、Ca2+、OH;氯化钡、氢氧化钙都过量:Na+、Cl、Ba2+、Ca2+、OH;故上层溶液中含有的离子最多可能有5种。
[分析讨论]碱性溶液能使酚酞溶液变红色,酸性溶液和中性溶液不能使酚酞溶液变色,故小红认为上层溶液中一定不含有H+,因为上层溶液呈红色或烧杯中有沉淀。小李取一定量的上层溶液于试管中,滴加几滴稀盐酸,发现无气泡产生,由于酸碱优先反应,如果所加盐酸过少,被碱全部消耗,则不能与碳酸根离子反应,则认为上层溶液中一定不含有CO32-的结论不正确,故原因是上层溶液中含 OH-时,滴加稀盐酸如果不足量也不会有气泡产生。
[设计实验]氯化钡和碳酸钠反应生成碳酸钡沉淀和氯化钠,试管中的上层溶液仍是红色,说明溶液显碱性,则大烧杯中的上层溶液中一定含有的阴离子是氢氧根离子。
实验操作 | 实验现象 | 实验结论 |
取大烧杯中的上层 溶液少许于一支试 管中,滴加足量(或过量)的BaCl2溶液, 静置 | 产生白色沉淀;试管中的上层溶液仍是红色 | 大烧杯中的上层溶液中一定含有CO32 ,发生的化学反应方程式为 |
[实验结论] 取大烧杯中的上层溶液少许于一支试管中,滴加足量(或过量)的BaCl2溶液, 静置,产生白色沉淀;试管中的上层溶液仍是红色,氯化钡和碳酸钠反应生成碳酸钡沉淀和氯化钠,说明上层溶液中含有碳酸钠,氢氧化钠,氯化钠,故大烧杯中的上层溶液中一定含有的离子是Na+、Cl-、CO32-、OH-。