��Ŀ����
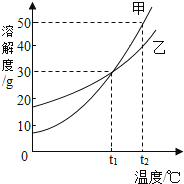
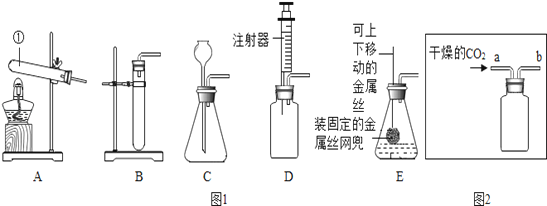
����Ŀ��ij��ѧ��ȤС�����ͼ1װ�ý���ģ��������ʵ�飬���������·�Ӧһ��ʱ�������ɷֺ�ʣ�����ɷֽ���̽���� 
��1��д��ͼ1װ�����漰�Ļ�ѧ����ʽ ��
��2�����۲������⡿�ù�������ɫ����a��ʲô��
��������Ԥ�⡿����1����ɫ����a ��CO2 ��
����2����ɫ����a�� ��
��3����ʵ������ʵ��
���ڵ�ȼͼ1װ�õľƾ����ǰ������ͨһ����̼һ��ʱ�䣬Ŀ���� ��
���ڱ�֤ʵ�鰲ȫ��ǰ���£�С�����ͼ2װ����֤���루װ��B�������dz�ȥCO2���壬װ��C�������dz�ȥ������ˮ�֣���ʵ���й۲쵽 �� �ɴ�С�ŵó����ۣ�����2������
��4�������������ۡ���Ӧһ��ʱ���ͼ1װ�õ�ʣ������п��ܳ��ֵĵ����� �� ����16gFe2O3���·�Ӧһ��ʱ���Ƶ�ʣ����������Ϊ12.8g��ͨ�������ȷ������ʱ����ɫ����a��һ������g�����壮
���𰸡�
��1��Fe2O3+3CO ![]() 2Fe+3CO2
2Fe+3CO2
��2��������̼��һ����̼
��3����ֹһ����̼�Ϳ�����ϼ���ʱ������ը������ʯ��ˮ����ǣ�β��ȼ����������������ɫ����
��4������8.8��������̼
���������⣺ͼ1װ�����漰�ķ�Ӧ����������һ����̼��Ӧ�������Ͷ�����̼����Ӧ�Ļ�ѧ����ʽΪ��Fe2O3+3CO ![]() 2Fe+3CO2 ��
2Fe+3CO2 ��
���Fe2O3+3CO ![]() 2Fe+3CO2 ��
2Fe+3CO2 ��
��������Ԥ�⡿
����1����ɫ����a ��CO2 ��
����2����ɫ����a�Ƕ�����̼��һ����̼��
���������̼��һ����̼��
��ʵ������ʵ��
���ڵ�ȼͼ1װ�õľƾ����ǰ������ͨһ����̼һ��ʱ�䣬Ŀ���Ƿ�ֹһ����̼�Ϳ�����ϼ���ʱ������ը��
�����ֹһ����̼�Ϳ�����ϼ���ʱ������ը��
��ʵ���й۲쵽����ʯ��ˮ����ǣ�β��ȼ����������������ɫ���棬�ɴ�С�ŵó����ۣ�����2������
�������ʯ��ˮ����ǣ�β��ȼ����������������ɫ���森
�����������ۡ�
��Ӧһ��ʱ���ͼ1װ�õ�ʣ������п��ܳ��ֵĵ���������
�����ɶ�����̼����Ϊx��
Fe2O3+3CO ![]() 2Fe + 3CO2 �� ������ٵ�����
2Fe + 3CO2 �� ������ٵ�����
160 112 132 160��112=48
x 16g��12.8g=3.2g![]()
x=8.8g��
����16gFe2O3���·�Ӧһ��ʱ���Ƶ�ʣ����������Ϊ12.8g����ʱ����ɫ����a��һ������8.8g�Ķ�����̼���壮
�������8.8��������̼��
�����㾫����������Ĺؼ���������һ����̼��ԭ�����������֪ʶ������ԭ�����ڸ����£����ý�̿��������Ӧ���ɵ�һ����̼����������ʯ�ﻹԭ�������Լ�����д��ѧ����ʽ�����ֱ���ʽ�����뷽��ʽ�����⣬�˽�ע�⣺a����ƽ b������ c�����ţ�