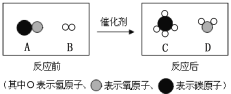
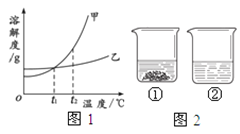
题目内容
【题目】(10分).某同学把MgSO4溶液、CuSO4溶液中分别加入铁粉中(如图实验一),实验结束后,把①、②试管内的物质集中倒进一个烧杯中(如图实验二)。请你回答下列有关问题:
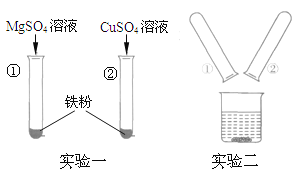
(1)实验一:发生反应的化学方程式是 ,从该实验可以得出三种金属的活动顺序从强到弱顺序是 。
(2)为探究实验二烧杯中物质的成分,该同学又进行如下实验过程:
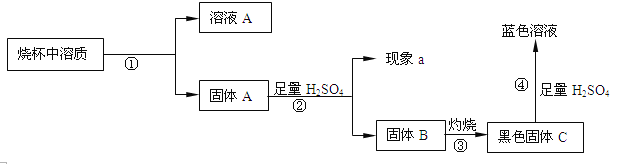
A.④的化学方程式是 。
B.若现象a产生气泡,则固体A是 ,溶液A的溶质是 ;若现象a无气泡,则固体A是 ,溶液A的溶质一定含有 ,可能含有 。
【答案】(1)Fe+CuSO4=Cu+FeSO4 Mg 、Fe、Cu(或用名称) (2)A:CuO+H2SO4=CuSO4+H2O B:Cu和Fe(有错、漏不得分) MgSO4、FeSO4(有错、漏不得分) Cu MgSO4、FeSO4 (有错、漏不得分) CuSO4
【解析】
试题分析:把MgSO4溶液、CuSO4溶液中分别加入铁粉中,铁只能和硫酸铜反应,方程式为Fe+CuSO4=Cu+FeSO4,从该实验可以得出三种金属的活动顺序从强到弱顺序是镁铁铜,④是黑色固体和足量硫酸反应生成硫酸铜,所以C为氧化铜,反应的方程式为CuO+H2SO4=CuSO4+H2O,现象a产生气泡,所以固体中有铁,有铁存在时,溶液中就不存在硫酸铜,所以固体A是铜和铁,溶液A是硫酸镁和硫酸亚铁,若现象a无气泡,则固体中没有铁,但是肯定有铜,溶液A中一定有硫酸镁,硫酸亚铁,因为一定发生的反应是铁和硫酸铜的反应,所以产物一定有硫酸亚铁,然后,硫酸铜可能还要,也可能已经被完全反应,所以是可能有硫酸铜。

练习册系列答案
相关题目