题目内容
将10 g不纯的锌粒(杂质不溶于水也不溶于酸)投入到100 g稀硫酸中完全反应,得到了0.2 g气体.试计算:
(1)锌粒的纯度;
(2)参加反应的稀硫酸的质量分数.
答案:

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
实验室用98%的浓硫酸配制成稀硫酸,并与锌粒反应制取氢气.
(1)查阅资料.
20℃时不同质量分数硫酸的密度(g/mL)
分析以上数据,可以得出结论(写2条)
①______;
②______;
(2)计算.
配制200g24.5%的稀硫酸,需______g98%浓硫酸和______ g水.实际操作时,取98%浓硫酸______ mL(精确到1mL);
(3)配制稀硫酸.
分别用量筒量取所需水和浓硫酸,先将______倒入烧杯中,然后______;
(4)制取氢气.
①如图中可用于制取、收集氢气的装置是(填字母)______;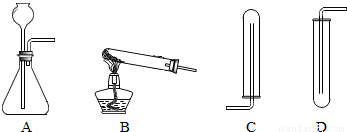
②检验氢气纯度的方法如图所示,标明氢气不纯的现象是______.
(1)查阅资料.
20℃时不同质量分数硫酸的密度(g/mL)
| 质量 分数 | 0% (纯水) | 1% | 4% | 10% | 16% | 24% | 32% | 36% | 44% | 49% | 60% | 98% |
| 密度 | 1.00 | 1.01 | 1.02 | 1.07 | 1.11 | 1.17 | 1.24 | 1.27 | 1.34 | 1.39 | 1.50 | 1.84 |
①______;
②______;
(2)计算.
配制200g24.5%的稀硫酸,需______g98%浓硫酸和______ g水.实际操作时,取98%浓硫酸______ mL(精确到1mL);
(3)配制稀硫酸.
分别用量筒量取所需水和浓硫酸,先将______倒入烧杯中,然后______;
(4)制取氢气.
①如图中可用于制取、收集氢气的装置是(填字母)______;

②检验氢气纯度的方法如图所示,标明氢气不纯的现象是______.