题目内容
乙醇发生不完全燃烧可表示为2C2H5OH+5O2 2CO+2CO2+6H2O假设得到燃烧的产物CO、CO2、H2O的总质量为27.6克,此中H2O的质量为10.8克,则产物中CO的质量为( )
2CO+2CO2+6H2O假设得到燃烧的产物CO、CO2、H2O的总质量为27.6克,此中H2O的质量为10.8克,则产物中CO的质量为( )
【答案】分析:根据可燃物乙醇发生不完全燃烧,其中氢元素全部生成水而碳元素生成了CO、CO2,利用化学变化前后元素质量不变,可由生成水的质量计算出燃烧的乙醇的质量;乙醇中所含碳元素的质量与燃烧产物CO、CO2中碳元素质量相等,利用两气体的总质量与其中碳元素总质量可计算其中含CO的质量.
解答:解:根据乙醇燃烧时其中氢元素全部生成水,生成H2O的质量为10.8g时燃烧乙醇的质量=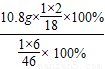 =9.2g
=9.2g
9.2g乙醇中C元素的质量=9.2g×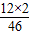 ×100%=4.8g
×100%=4.8g
总质量为27.6克燃烧的产物中CO、CO2的总质量=27.6g-10.8g=16.8g,设其中CO的质量为y,则
y× ×100%+(16.8g-y)×
×100%+(16.8g-y)×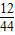 ×100%=4.8g
×100%=4.8g
y=1.40g
故选A.
点评:解答本题时需要注意,题中所给的反应并不是实际发生反应的化学方程式,只能从中得出燃烧时乙醇中氢元素全部生成了水的结论,不能把它当作反应的化学方程式而根据它进行计算.
解答:解:根据乙醇燃烧时其中氢元素全部生成水,生成H2O的质量为10.8g时燃烧乙醇的质量=
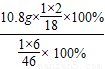 =9.2g
=9.2g9.2g乙醇中C元素的质量=9.2g×
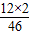 ×100%=4.8g
×100%=4.8g总质量为27.6克燃烧的产物中CO、CO2的总质量=27.6g-10.8g=16.8g,设其中CO的质量为y,则
y×
 ×100%+(16.8g-y)×
×100%+(16.8g-y)×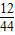 ×100%=4.8g
×100%=4.8g y=1.40g
故选A.
点评:解答本题时需要注意,题中所给的反应并不是实际发生反应的化学方程式,只能从中得出燃烧时乙醇中氢元素全部生成了水的结论,不能把它当作反应的化学方程式而根据它进行计算.

练习册系列答案
相关题目
乙醇发生不完全燃烧可表示为2C2H5OH+5O2
2CO+2CO2+6H2O假设得到燃烧的产物CO、CO2、H2O的总质量为27.6克,此中H2O的质量为10.8克,则产物中CO的质量为( )
| ||
| A、1.40克 | B、6.53克 |
| C、16.8克 | D、不确定 |
 2CO+2CO2+6H2O假设得到燃烧的产物CO、CO2、H2O的总质量为27.6克,此中H2O的质量为10.8克,则产物中CO的质量为
2CO+2CO2+6H2O假设得到燃烧的产物CO、CO2、H2O的总质量为27.6克,此中H2O的质量为10.8克,则产物中CO的质量为 2CO+2CO2+6H2O假设得到燃烧的产物CO、CO2、H2O的总质量为27.6克,此中H2O的质量为10.8克,则产物中CO的质量为( )
2CO+2CO2+6H2O假设得到燃烧的产物CO、CO2、H2O的总质量为27.6克,此中H2O的质量为10.8克,则产物中CO的质量为( )