题目内容
某兴趣小组在密闭容器中分别将1.2g镁放在一定量氧气中燃烧,得如下实验数据:
第一次所给氧气的质量为0.4g,生成氧化镁的质量为1.0g;
第二次所给氧气的质量为0.8g,生成氧化镁的质量为2.0g;
第三次所给氧气的质量为1.6g,生成氧化镁的质量为2.0g.
下列实验分析错误的是( )
第一次所给氧气的质量为0.4g,生成氧化镁的质量为1.0g;
第二次所给氧气的质量为0.8g,生成氧化镁的质量为2.0g;
第三次所给氧气的质量为1.6g,生成氧化镁的质量为2.0g.
下列实验分析错误的是( )
| A、第一次实验中镁没有燃烧完 | B、只有第二次实验遵守质量守恒定律 | C、第三次实验中氧气没有消耗完 | D、三次实验后固体质量都增加了 |
分析:在本题中,根据化学方程式的计算,1.2g镁与0.8g氧气恰好完全反应,因此第一次实验中镁没有燃烧完;第二次是恰好完全反应;第三次实验中氧气没有消耗完;三次都遵守质量守恒定律,实验后固体质量都增加了.
解答:解:设1.2g镁需要氧气的质量为x
2Mg+O2
2MgO
48 32
1.2g x
=
x=0.8g
因此第一次实验中镁没有燃烧完;第二次是恰好完全反应;第三次实验中氧气没有消耗完;三次都遵守质量守恒定律,实验后固体质量都增加了.
故答案为:B
2Mg+O2
| ||
48 32
1.2g x
| 48 |
| 1.2g |
| 32 |
| x |
因此第一次实验中镁没有燃烧完;第二次是恰好完全反应;第三次实验中氧气没有消耗完;三次都遵守质量守恒定律,实验后固体质量都增加了.
故答案为:B
点评:本考点考查了根据化学方程式的计算,属于质量守恒定律和化学方程式的综合应用,是中考计算题中经常出现的题型.做题时要注意:化学方程式要写正确,始终不要忘记质量守恒定律,本考点主要出现在计算题中.

练习册系列答案
相关题目
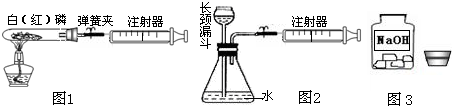
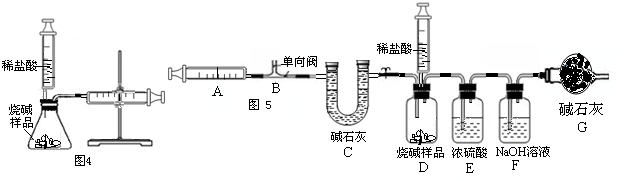
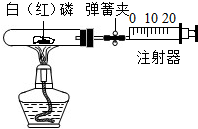 某化学兴趣小组的同学对教材中“测定空气里氧气含量”的实验做了改进,在密闭容器里进行磷的燃烧,以防止产生的白烟污染空气.他们设计了图示实验:选用容积为50mL的试管作反应容器,选用50mL的注射器(开始时活塞处于20mL刻度处)来测量磷燃烧时所消耗氧气的体积.
某化学兴趣小组的同学对教材中“测定空气里氧气含量”的实验做了改进,在密闭容器里进行磷的燃烧,以防止产生的白烟污染空气.他们设计了图示实验:选用容积为50mL的试管作反应容器,选用50mL的注射器(开始时活塞处于20mL刻度处)来测量磷燃烧时所消耗氧气的体积.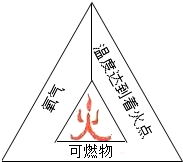 通常情况下,燃烧需要三个条件,如图所示.
通常情况下,燃烧需要三个条件,如图所示.