题目内容
将锌片和铜片用导线连接后放入稀硫酸溶液中发生原电池反应,下列叙述正确的是( )
A.负极附近的SO42-浓度逐渐减小
B.正极有O2逸出
C.电子通过导线由铜片流向锌片
D.铜片上有H2逸出
同学们运用对比的学习方法探究碱的性质.
实验一 | 实验二 | 实验三 |
观察固体表面
| 向两块固体表面滴加稀盐酸
| 振荡三个塑料瓶
|
(1)由如图实验一、二可知,氢氧化钠会吸收空气的________,因此要密封保存.
(2)实验三中可观察到三个软塑料瓶变瘪的程度大小为A>B>C,A瓶内发生反应的化学方程式为________,对比A瓶与________(选填“B”或“C”)瓶的实验现象可证明CO2能与NaOH发生反应.
(3)同学们设计如下两种方案鉴别氢氧化钠溶液与氢氧化钙溶液(分别编号为A、B).
方案一 | 方案二 | 分析 |
|
| 两种方案中均观察到A试管内出现白色浑浊,A中试剂为________;方案二的A溶液变浑浊的原因是________. |
(4)同学们看到盛有NaOH的试剂瓶上标注着“NaOH含量不少于96.0%”,开始如下探究:
(提出问题)氢氧化钠中含有什么杂质?
(查阅资料)①在化工生产中,原料往往不能全部转化为产品.
②工业制取NaOH的反应原理是:2NaCl+2H2O ?2NaOH+H2↑+Cl2↑,然后蒸发溶剂获得NaOH固体.
?2NaOH+H2↑+Cl2↑,然后蒸发溶剂获得NaOH固体.
③碱性的Na2CO3溶液与中性的CaCl2溶液发生复分解反应.
(提出猜想)氢氧化钠中含有的杂质为碳酸钠和氯化钠.提出上述猜想的理由是________.
(实验探究)取样溶于水,并分成两份.
步骤I:向一份溶液中滴加酚酞试剂;
步骤II:向另一份溶液中滴加过量稀盐酸;
(实验结论)两份溶液中均有明显现象,证明杂质中一定含有碳酸钠.
(反思评价)上述实验中步骤________(填写序号)是没有必要进行的.
实验是科学探究的重要方法。如图是测定空气中氧气含量实验的两套装置图,请结合图示回答有关问题。
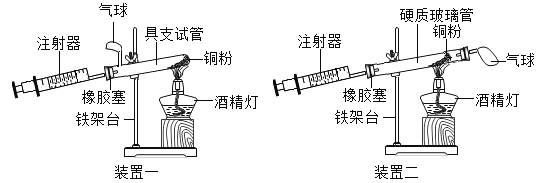
(1)在装置二中,根据下表提供的实验数据,完成下表。
硬质玻璃管中空气的体积 | 反应前注射器中空气体积 | 反应后注射器中气体体积 | 实验测得空气中氧气的体积分数 |
20mL | 10 mL | 5 mL | ____ |
(2)装置一和装置二中气球的位置不同,________(填“装置一”或“装置二”)更合理,理由是________ 。
(3)若实验测得的结果偏小(氧气的体积分数小于21%),可能的原因有哪些?(列举两条)________;________。
(4)加热时,硬质玻璃管里发生反应的现象________,反应的文字表达式为________,该反应的基本类型是________。