题目内容
将等质量的镁和锌分别放入等浓度、等质量的稀盐酸中,充分反应后发现两种金属都有剩余,则它们生成氢气的量( )
| A、镁多 | B、锌多 |
| C、镁和锌一样多 | D、无法判断 |
考点:金属的化学性质
专题:金属与金属材料
分析:等质量的Mg与Zn与质量相同、溶度相同的稀盐酸完全反应,酸完全反应最终产生氢气的质量相等,因为氢气最终来源于酸中的氢元素.
解答:解:金属有剩余则说明酸已完全反应,由于氢气来源于酸中的氢元素,所以生成的氢气应该是相等的.
故选C.
故选C.
点评:本题考查了金属与酸反应的速度以及产生氢气质量的关系,完成此题,可以依据已有的知识.所以要求同学们在平时的学习中加强基础知识的记忆和理解,以便能够灵活应用.

练习册系列答案
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
现有氢气、二氧化碳、甲烷三种气体,若用最简单的方法将它们鉴别出来,除用火柴外,至少还需要下列试剂中的( )
| A、浓硫酸 | B、酚酞试液 |
| C、澄清的石灰水 | D、氢氧化钠溶液 |
98春节期间山西省朔州市发生了震惊全国的假酒案,有数百人因饮用假酒而中毒,有的眼睛失明,有的死亡了,假酒中使人中毒的物质是( )
| A、乙醇 | B、甲醇 |
| C、醋酸 | D、一氧化碳 |
除去下列各物质中少量的杂质的方法,正确的是( )
| 选项 | 物质 | 杂质 | 除去杂质的办法 |
| A | CO2 | CO | 通入氧气,点燃 |
| B | N2 | O2 | 通过灼热的铜网 |
| C | CO2 | HCl | 通过装有NaOH溶液的洗气瓶 |
| D | H2 | 水蒸气 | 适量的稀硫酸 |
| A、A | B、B | C、C | D、D |
日常生活中的许多现象与化学反应有关,下列现象与氧化还原反应无关的是( )
| A、铜铸塑像上出现铜绿[Cu2(OH)2CO3] |
| B、铁制菜刀生锈 |
| C、大理石雕像被酸雨腐蚀毁坏 |
| D、铝锅表面生成致密的薄膜 |
下列叙述的微观解释中,不正确的是( )
| A、CO和CO2的化学性质不同--二者的分子构成不同 |
| B、用警犬搜救地震中的被埋人员--分子在不断地运动 |
| C、化学反应遵守质量守恒定律--化学反应前后原子的种类、数目、质量没有改变 |
| D、水烧开后易把壶盖冲起--温度升高,分子变大 |
下列物质之间的转化,经过两步反应仍不能达到目的是( )
| A、C→H2CO3 |
| B、CuO→Cu(OH)2 |
| C、Na→NaOH |
| D、CaCO3→NaOH |
下列家庭小实验不能制得溶液的是( )
A、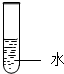 食盐 |
B、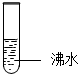 饱和FeCl3溶液 |
C、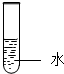 蔗糖 |
D、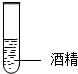 碘 |