题目内容
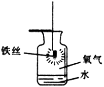
【题目】利用图甲装置探究“MnO2的用量对H2O2分解反应的影响”,实验中H2O2的溶质质量分数为3%,装置中产生氧气的量可以用压强传感器测出(在等温条件下,产生氧气体积与装置内压强成正比。反应放热忽略不计。)
(1)写出装置中发生反应的化学方程式: ,MnO2在此反应中起 作用。
(2)图乙是“0.1克MnO2与不同体积的3%H2O2溶液混合”的实验结果,从图中可以看出 。
(3)当用“3%H2O2溶液8毫升与不同质量的MnO2混合”时,得到如图丙所示的曲线。曲线的斜率显示,当MnO2的用量增加到0.08克时,分解速度达到实验要求。在此实验条件下,若MnO2的质量有4克(一药匙),就能使下图 (选填字母)烧杯中所装的3%H2O2溶液,其分解速度最接近实验要求。
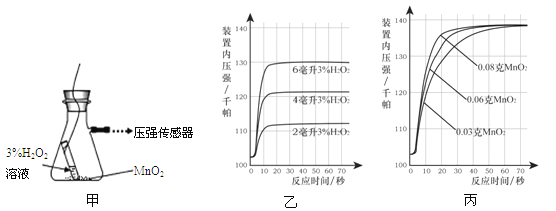
【答案】(1)2H2O2 ![]() 2H2O +O2↑ 催化
2H2O +O2↑ 催化
(2)H2O2的用量越多,产生的氧气越多 (3)C
【解析】
试题分析:装置的物质过氧化氢,过氧化氢可以在二氧化锰做催化剂的条件下反应快速反应,反应的化学方程式:2H2O2 ![]() 2H2O +O2↑;MnO2在此反应中起催化作用;图乙是“0.1克MnO2与不同体积的3%H2O2溶液混合”的实验结果,从图中可以看出H2O2的用量越多,产生的氧气越多;当用“3%H2O2溶液8毫升与不同质量的MnO2混合”时,得到如图丙所示的曲线。曲线的斜率显示,当MnO2的用量增加到0.08克时,分解速度达到实验要求,说明二者在比例为100:1的情况下反应最好。因此当MnO2的质量有4克时,过氧化氢的质量最好为400毫升。故选C。
2H2O +O2↑;MnO2在此反应中起催化作用;图乙是“0.1克MnO2与不同体积的3%H2O2溶液混合”的实验结果,从图中可以看出H2O2的用量越多,产生的氧气越多;当用“3%H2O2溶液8毫升与不同质量的MnO2混合”时,得到如图丙所示的曲线。曲线的斜率显示,当MnO2的用量增加到0.08克时,分解速度达到实验要求,说明二者在比例为100:1的情况下反应最好。因此当MnO2的质量有4克时,过氧化氢的质量最好为400毫升。故选C。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目