题目内容
【题目】随着生产的发展,家庭日用品的种类也日益增多。以下是几种常见的清洁剂。

(1)彩漂液的有效成分为过氧化氢,长期存放会因分解而失效。用化学方程式解释失效的原因________。
(2)“洁厕灵”的有效成分是稀盐酸,不小心滴到大理石地面上,发现有气泡产生,发生反应的方程式为 __________。
(3)“管道通”中的有效成分是氢氧化钠,它不能与“洁厕灵”混合使用,其原因是________(用化学方程式表示)。
【答案】2H2O2=2H2O+O2↑ CaCO3 +2HCl=CaCl2+H2O+CO2 ↑ NaOH+HCl=NaCl+H2O
【解析】
(1)过氧化氢常温下分解生成水和氧气,反应的化学方程式为:2H2O2=2H2O+O2↑.
(2)大理石的主要成分是碳酸钙,与稀盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑.
(3)氢氧化钠与稀盐酸发生中和反应,生成氯化钠和水,反应的化学方程式为:NaOH+HCl=NaCl+H2O.
故答案为:(1)2H2O2=2H2O+O2↑;(2)CaCO3+2HCl=CaCl2+H2O+CO2↑;(3)NaOH+HCl=NaCl+H2O.

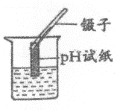
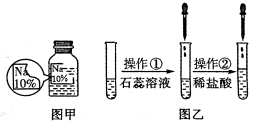
【题目】(7分)某同学在实验室发现了一瓶标签残缺的无色溶液﹙如图甲所示﹚,为确认其中的溶质,他设计并进行了如下探究活动,请回答下列问题。
【猜想与假设】其溶质可能为NaCl、NaOH、Na2CO3和NaHCO3中的一种。
【资料查阅】上述四种物质的相关信息如下:
物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
常温下的溶解度/g | 36 | 109 | 21.5 | 9.6 |
常温下某稀溶液的pH | 7 | 13 | 11 | 9 |
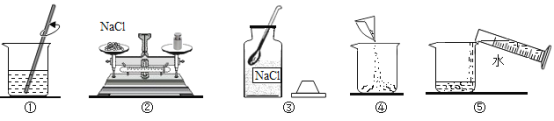
【探究过程】
如图乙所示,在操作①后可确定溶质不是NaCl,则其实验现象应是 ;
在进行操作②时有无色无味得到气体产生,由此又可排除假设物质中的 。
【探究结论】
你认为该溶液中的溶质可能是上述假设物质中的 ,你的判断依据是 。
【探究反思】
(1)若上述探究结论是正确的,操作②产生的气体应是 (写化学式),实验室检验该气体的实验操作及现象是 。
(2)另有同学猜想其中的溶质还可能是Na2SO4,但又没有Na2SO4的上述表列信息。
请你根据以上实验操作的相关现象,判断该溶液中的溶质是否是Na2SO4,并叙述理由: 。