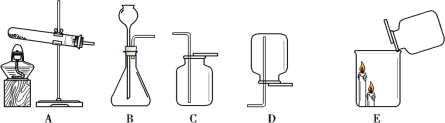题目内容
【题目】小冬同学制作的简易净水器如图所示:
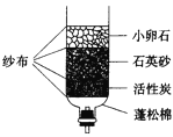
(1)小卵石、石英砂和膨松棉的作用是_____________,活性炭的作用是_____。
(2)净化后是硬水还是软水?可用_____来检验。
(3)长期饮用硬水对人体不利,可采用_____的方法降低水的硬度。
【答案】过滤 吸附水中的色素和异味 肥皂水 加热煮沸或蒸馏
【解析】
(1)小卵石、石英沙和膨松棉可以除去水中的一些不溶性杂质,起了过滤的作用,活性炭可吸附水中的色素和异味;
(2)向水中加入肥皂水时,如果产生大量的泡沫,说明是软水;如果产生的泡沫很少,说明是硬水。净化后的水可用肥皂水来检验;
(3)水样加热煮沸时,水中可溶性钙、镁化合物转化为沉淀,水的硬度降低;蒸馏能除去水中所有的杂质。加热煮沸或蒸馏可以降低水的硬度。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目