��Ŀ����
����Ŀ�����������ʵ��װ��ͼ�ش����⡣
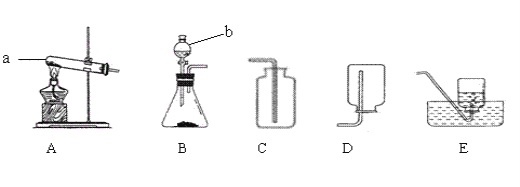
(1)д������a��b�����ƣ�a��________��b��________
(2)ʵ�����ü����Ȼ�狀��������ƹ�������ķ�����ȡ������NH3����ͬʱ�õ��Ȼ��ƺ�ˮ���÷�Ӧ�Ļ�ѧ����ʽ��_______________��Ӧѡ�õķ���װ��Ϊ____����װ�ñ�ţ���
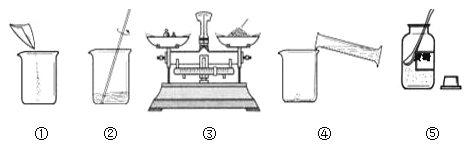
(3)�ռ�����ʱӦѡ��Dװ�ã����ռ��������ļ���ƿ�����ڵ� ����ɫ��̪��Һ��ˮ���У��۲쵽����ƿ���д�����ɫҺ����롣
����������Ϣ�ܽ��������������_______��_________���ش��������ɣ���
���𰸡���1���Թ� ��Һ©��
��2��2H2O2![]() 2H2O+O2��
2H2O+O2��
��3��2NH4Cl+Ca��OH��2![]() CaCl2+2NH3��+2H2O A
CaCl2+2NH3��+2H2O A
��4���������ܶȱȿ���С ������������ˮ�γɰ�ˮ
�������������������1��������������ͼ��a���Թܣ�b�Ƿ�Һ©�����ʴ�Ϊ���Թܣ���Һ©����
��2��Bװ�������ڹ����Һ��IJ����ȷ�Ӧ����ȡ����ʱ���ö��������������ֽ����������Һ����ѧ��Ӧ����ʽ�ǣ�2H2O2![]() 2H2O+O2����
2H2O+O2����
��3���Ƶð������ü����Ȼ�狀��������ƹ�������ķ����������������������������ѡ��A����ѧ��Ӧ����ʽ�ǣ�2NH4Cl+Ca��OH��2![]() CaCl2+2NH3��+2H2O��
CaCl2+2NH3��+2H2O��
��4���ռ�����ʱӦѡ��Dװ�ã�˵���������ܶ�С�ڿ������ܶȣ���ˮ�Լ��ԣ�������Һ��ʹ��̪��Һ��죬����ƿ���д�����ɫҺ����룬˵��������������ˮ�γɰ�ˮ���ʴ�Ϊ���������ܶȱȿ���С��������������ˮ�γɰ�ˮ��