题目内容
配制500mL的质量分数为10%的氢氧化钠溶液(密度为1.1g/cm3),需要氢氧化钠和水的质量各是多少?
【答案】分析:配制一定量的溶液所需溶质的质量=溶液质量×溶质的质量分数;
根据溶液的组成,配制溶液所需溶剂水的质量=溶液质量-溶质质量.
解答:解:配制500mL的质量分数为10%的氢氧化钠溶液,需要氢氧化钠的质量=500mL×1.1g/cm3×10%=55g;
需要水的质量=500mL×1.1g/cm3-55g=495g
答:需要氢氧化钠和水的质量分别为55g和495g.
点评:根据公式:溶液中溶质质量分数=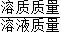 ×100%,已知任意两个量都可计算出另外一个量.
×100%,已知任意两个量都可计算出另外一个量.
根据溶液的组成,配制溶液所需溶剂水的质量=溶液质量-溶质质量.
解答:解:配制500mL的质量分数为10%的氢氧化钠溶液,需要氢氧化钠的质量=500mL×1.1g/cm3×10%=55g;
需要水的质量=500mL×1.1g/cm3-55g=495g
答:需要氢氧化钠和水的质量分别为55g和495g.
点评:根据公式:溶液中溶质质量分数=
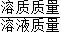 ×100%,已知任意两个量都可计算出另外一个量.
×100%,已知任意两个量都可计算出另外一个量. 
练习册系列答案
相关题目